Lär dig viktiga kunskaper om kosttillskott med vår guide om de tre bästa naturliga senolytika som kan föryngra cellerna och förbättra hälsan. När vi åldras kan cellulär senescens - där cellerna slutar dela sig och ansamlas i kroppen - leda till olika åldersrelaterade sjukdomar. Vissa naturliga föreningar har dock identifierats som kraftfulla senolytika som selektivt kan rensa bort dessa åldrade celler. I den här artikeln går vi djupare in på vetenskapen bakom dessa anmärkningsvärda ämnen och hur man kan införliva dem i de dagliga rutinerna för att uppnå åldersförbättrande hälsofördelar.
Introduktion till ämnet
Åldrande är en komplex biologisk process som kännetecknas av en gradvis försämring av fysiologiska funktioner och en ökad känslighet för sjukdomar. Åldrandet har länge betraktats som en oundviklig aspekt av livet, men de senaste framstegen inom biogerontologi har avslöjat cellulära och molekylära mekanismer som ligger bakom åldrandet. Bland dessa mekanismer har cellulär senescens framstått som en viktig bidragande orsak till åldersrelaterade sjukdomar. Det är ett irreversibelt tillväxtstopp som utlöses av olika stressfaktorer.(1)
Eftersom antalet senescenta celler ökar med stigande ålder har man antagit att senescens bidrar till åldrandet. Senescens behövs för att förhindra spridning och proliferation av skadade celler, vilket utlöser en reaktion från immunförsvaret. Denna cellulära kontrollpunkt kräver ett effektivt cellutbytessystem som innefattar både rensning av senescenta celler och mobilisering av progenitorceller för att återställa ett optimalt cellantal.(2)
Skador på DNA-kärnan rapporteras ofta som en bakomliggande orsak till senescens, främst i form av dubbelsträngsbrott (DSB) som aktiverar DDR-vägen (DNA damage response). Långvarig DDR-aktivering aktiverar senescens. En eller ett fåtal DDR-signalerande telomerer (kromosomändar) är tillräckliga för att utlösa replikativ cellsenescens. Onkogen aktivering är också en stark senescensutlösande faktor.(3)
Senescenta celler uttrycker betydande förändringar i sin sekretom, som är särskilt berikad med proinflammatoriska cytokiner och matrismetalloproteinaser. Den kallas därför den senescensassocierade sekretoriska fenotypen (SASP).. Senescenta celler uppvisar distinkta fenotypiska förändringar, t.ex. tillplattad morfologi, förändrat genuttryck och utsöndring av proinflammatoriska molekyler. Även om senescens initialt fungerar som en tumörhämmande mekanism genom att stoppa spridningen av skadade celler, bidrar ackumuleringen av senescenta celler över tid till vävnadsdysfunktion och främjar åldersrelaterade sjukdomar. (4)
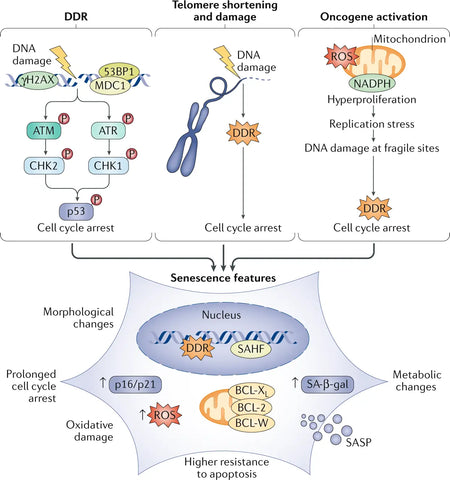
Bild: Drivkrafter och fenotyper för senescens.
Källan: Di Micco, R., Krizhanovsky, V., Baker, D., & d'Adda di Fagagna, F. (2021). Cellulär senescens i åldrandet: från mekanismer till terapeutiska möjligheter. Nature Reviews Molekylär cellbiologi 22 (2): 75–95.
Med tanke på de skadliga effekterna av senescenta celler på vävnadshomeostas och hälsospan har inriktning på dessa celler framstått som en lovande terapeutisk strategi. Senolytika är föreningar som är utformade för att framkalla apoptos i senescenta celler samtidigt som de selektivt skonar friska celler. De har potential att lindra inflammation, förbättra vävnadsregenerering och fördröja uppkomsten av åldersrelaterade sjukdomar.(5)
Senolytiska föreningar
Ett stort antal naturliga och syntetiska föreningar har identifierats som potentiella senolytikadär quercetin (en naturlig förening) och dasatinib (ett syntetiskt läkemedel) utgör tidiga kandidater i denna klass. Förutom quercetin och dasatinib har flera andra föreningar, däribland fisetin, navitoclax och ABT-263, har visat lovande senolytiska egenskaper i prekliniska modeller. I denna artikel beskrivs de 3 mest potentiella och lovande naturliga senolytika som finns tillgängliga idag.
Fisetin
Fisetin är en bioaktiv flavonol (en polyfenol) som studerats avsevärt för sin potential att främja hälsa och livslängd, främst genom att mildra cellulär senescens. Det finns främst i jordgubbar, äpplen, persimoner, lök, druvor och i små mängder i gurka (se bild). Fisetin har en rad olika biologiska aktiviteter som kan hänföras till dess unika molekylstruktur (en plan struktur och flera kolringar).(6-7)
En första undersökning av Fisetins egenskaper avslöjar dess potenta antioxidantkapacitet, som härrör från dess förmåga att rensa bort reaktiva syrearter (ROS). Således spelar det en avgörande roll i cellulärt försvar mot oxidativ stress.(8)

Bild: Kostkällor för fisetin.
Källor: Khan, N. & Syed, D. & Ahmad, N. & Mukhtar, H. (2013). Fisetin: en kostantioxidant för hälsofrämjande. Antioxidanter och redoxsignalering 19 (2): 151–162.
Fisetins senolytiska aktivitet utgör ett primärt fokus inom livslängdsforskningen. Cellulär senescens är ett tillstånd där celler upphör att proliferera och ackumuleras över tid - det är involverat i olika åldersrelaterade sjukdomar (se tidigare i mer detalj). Fisetin har visat sig inducera apoptos i dessa senescenta celler selektivt. Denna selektiva clearance antas lindra senescensassocierade fenotyper och därigenom bidra till fördröjning eller förebyggande av åldersrelaterade patologier. Jämfört med en annan möjlig senolytisk förening är Fisetin ungefär två gånger mer potent än quercetin (se senare i artikeln).(9-10)
Den prooxiderande aktiviteten hos flavonoider (som fisetin) är en viktig faktor vid screening för senolytika. Senescenta celler ackumulerar höga halter av koppar och järn. Den selektiva mekanismen för quercetin eller fisetin är uttryckligen förknippad med koppar-/järnpromotorerad oxidativ skada i senescenta celler och dödar därmed apoptosresistenta celler.(11)
Fisetin påverkar också viktiga cellulära signalvägar som är en integrerad del av åldringsprocessen. Det modulerar funktionen hos sirtuiner (särskilt SIRT1), mTOR (hämning) och JAK-STAT/NF-κB, som är avgörande för att reglera cellulär överlevnad, apoptos och autofagi. Genom att modulera dessa vägar kan Fisetin teoretiskt förbättra cellulär funktion, minska inflammation och upprätthålla vävnadshomeostas.(12-14)
Fisetin har också visat sig ha neuroprotektiva egenskaper. Det mildrar neuronal skada och förbättrar kognitiva funktioner, främst genom dess antioxidativa verkan och modulering av neuronala signalvägar.(15-16)
Trots dessa lovande prekliniska resultat är det viktigt att erkänna att den mesta forskningen om Fisetin har varit begränsad till in vitro- och djurmodeller. För att överföra dessa resultat till kliniska tillämpningar på människor krävs rigorösa kliniska prövningar för att fastställa Fisetins effekt, säkerhet och optimala dosering. Lyckligtvis är vissa kliniska studier redan på väg, och vi bör få resultat inom de närmaste åren.(17-18)
Quercetin
Quercetin är en viktig antioxidant som kategoriseras som en flavonol. Den förekommer naturligt i många grönsaker, frukter, bär, blad och sädesslag. Quercetin finns främst i kapris, rädisor, dill, koriander, kål, rödlök, broccoli och bär som tranbär och lingon. Quercetin är en av de mest betydelsefulla och vanliga flavonolerna som förekommer i naturen.

Forskning visar att quercetin fungerar som ett antiviralt, antimikrobiellt och antiinflammatoriskt medel.(19) Dessutom har studier visat att quercetin har antihistamineffekter, vilket innebär att det kan hjälpa till att behandla allergier.(20-21) Den mest betydande effekten av quercetin på människokroppen är dess förmåga att minska tyst inflammation.(22)
Quercetins potential att främja livslängd kan hänföras till dess antioxidantegenskaper. Som antioxidant tar quercetin bort fria radikaler, vilket minskar den oxidativa stressen i kroppen. Forskning har visat att quercetin kan aktivera sirtuiner (särskilt SIRT-1), som reglerar cellulära processer som DNA-reparation, genuttryck och metabolism. Aktiveringen av sirtuiner är kopplad till ökad livslängd hos olika organismer.(23-24)
Quercetin har också visat sig aktivera Nrf2-vägen, och i cellkärnorna aktiverar det transkriptionen av olika ARE-styrda gener (antioxidant response element). Dessa gener uppreglerar uttrycket av cytoprotektiva enzymer, såsom glutation-S-transferas, NAD(P)H-kinondehydrogenas 1 och hemeoxygenas-1.(25)
Vanligtvis tas quercetintillskott i en dos av 500 mg två gånger om dagen. Den optimala dosen av quercetin har dock ännu inte fastställts. Det rekommenderade dagliga intaget av quercetin är vanligtvis 5-40 mg, men det kan också intas i betydligt större mängder (> 500 mg).
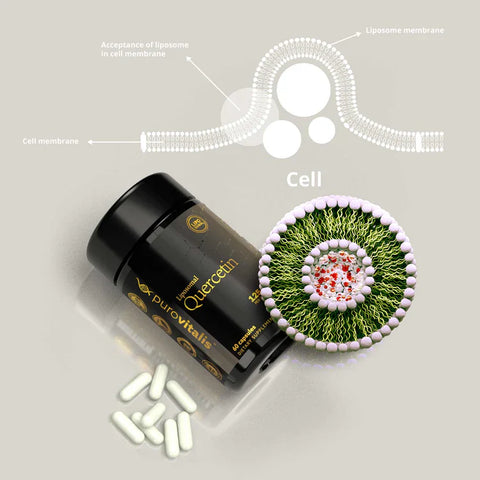
När det gäller quercetin är vår rekommendation den liposomala formen av Purovitalis.
Apigenin
Apigenin (4′,5,7,-trihydroxyflavone) är en naturligt förekommande flavonoidförening i olika växter, inklusive persilja, selleri och citrusfrukter. Det är särskilt rikligt i blommorna på kamomillväxten. Apigenin har potential att bidra till att förebygga kroniska sjukdomar som diabetes, Alzheimers, depression, sömnlöshet och cancer, med fördelar som observerats i vivo-forskning (djur- och humanstudier).(26)

En av de mest lovande aspekterna av apigenin är dess förmåga att främja cellulär motståndskraft. Apigenin har visat sig aktivera Nrf2-signalvägen, som är avgörande för kroppens försvar mot oxidativ stress och inflammation. Genom att uppreglera uttrycket av antioxidantenzymer som superoxiddismutas, katalas och glutationperoxidas bidrar apigenin till att skydda cellerna från skador som orsakas av reaktiva syreföreningar (ROS).(27)
Förutom sina antioxidativa egenskaper har apigenin visat sig ha antiinflammatoriska effekter. Det har visat sig att det hämmar produktionen av proinflammatoriska cytokiner, såsom TNF-α, IL-1β och IL-6, genom att modulera NF-κB-signalvägen.28) Apigenin har också undersökts för sina potentiella anti-cancer egenskaper. Studier har visat att apigenin kan inducera apoptos (programmerad celldöd) i olika cancercellinjer, inklusive bröst-, prostata- och koloncancerceller. Apigenin främjar också autofagi och hjälper därmed till att ta bort dysfunktionella cellulära element.(29-30)
Apigenin har också studerats för sin förmåga att modulera vägar som är förknippade med åldrande. En sådan väg är insulin/IGF-1-signalvägen (IIS), som är känd för att spela en roll i regleringen av livslängden hos olika arter. Apigenin har visat sig hämma IIS-vägen, vilket potentiellt kan efterlikna effekterna av kalorirestriktion, en väletablerad intervention för att främja livslängd.(31-32) Dessutom hämmar apigenin NAD+-asen CD38, som är förknippad med metabolt syndrom, vilket ökar de intracellulära NAD+-nivåerna och minskar den globala proteinacetyleringen.(33) När det gäller senescens, i synnerhet, har apigenin till att hämma kvarvarande senescenta celler från att bilda SASP (senescence associated secretory phenotype; se tidigare) för att stödja cell- och vävnadshälsa.(34)
När det gäller dosering finns det ingen allmänt rekommenderad dos för apigenintillskott. I studier har dock doser från 25 till 100 mg/kg kroppsvikt använts i djurmodeller.(35) Kosttillskott varierar vanligtvis från 50 till 500 mg per dag. Den mest effektiva och säkra dosen har dock ännu inte fastställts slutgiltigt. Apigenin anses i allmänhet vara säkert, men höga doser kan interagera med vissa mediciner.
Slutsats
Som avslutning på analysen av potentialen hos naturliga senolytika är det uppenbart att föreningar som fisetin, quercetin och apigenin uppvisar betydande senolytiska förmågor som kan påverka åldringsprocessen på ett djupgående sätt. Dessa substanser riktar sig specifikt mot och eliminerar senescenta celler och tar därmed itu med en grundläggande åldringsmekanism och relaterade patologier. Att integrera dessa bioaktiva föreningar i sin kost - från källor som jordgubbar, lök och kamomill - är ett strategiskt tillvägagångssätt för att förbättra cellfunktionen och mildra ackumuleringen av cellskador över tid.
Även om de prekliniska uppgifterna är lovande krävs det dock ytterligare empirisk forskning för att validera effekt och säkerhet om dessa resultat ska kunna omsättas i praktiska kliniska strategier. Därför är det viktigt att fortsätta utforska dessa substanser i rigorösa kliniska prövningar.
Vetenskapliga referenser:
- Sikora, E., Arendt, T., Bennett, M., & Narita, M. (2011). Inverkan av cellulära senescenssignaturer på åldrandeforskningen. Översikter över forskning om åldrande, 10(1), 146-152.
- He, S., & Sharpless, N. E. (2017). Senescens i hälsa och sjukdom. Cell, 169(6), 1000-1011.
- Di Micco, R., Krizhanovsky, V., Baker, D., & d'Adda di Fagagna, F. (2021). Cellulär senescens i åldrandet: från mekanismer till terapeutiska möjligheter. Nature Reviews Molekylär cellbiologi 22 (2): 75–95.
- Kuilman, T. & Michaloglou, C. & Mooi, W. & Peeper, D. (2010). Essensen av senescens. Gener och utveckling 24 (22): 2463–2479.
- Kirkland, J. L., & Tchkonia, T. (2020). Senolytiska läkemedel: från upptäckt till översättning. Journal of internal medicine, 288(5), 518-536.
- Sengupta, B. & Banerjee, A. & Sengupta, P. (2005). Interaktioner mellan växtflavonoiden fisetin och makromolekylära mål: insikter från fluorescensspektroskopiska studier. Journal of Photochemistry and Photobiology B: Biology 80 (2): 79–86.
- Bag, S. & Ghosal, S. & Karmakar, S. & Pramanik, G. & Bhowmik, S. (2023). Avslöja det kontrasterande bindningsbeteendet hos växtflavonoiderna Fisetin och Morin som har sekundära hydroxylgrupper (- OH) med HRAS1 och HRAS2 i-Motif DNA-strukturer: Avkodning av strukturella förändringar och positionella influenser. ACS Omega 8 (33): 30315–30329.
- Khan, N. & Syed, D. & Ahmad, N. & Mukhtar, H. (2013). Fisetin: en kostantioxidant för hälsofrämjande. Antioxidanter och redoxsignalering 19 (2): 151–162.
- Yousefzadeh, M. et al (2018). Fisetin är ett senoterapeutiskt medel som förlänger hälsa och livslängd. EBioMedicin 36: 18-28.
- Wyld, L. et al (2020). Senescens och cancer: en genomgång av kliniska konsekvenser av senescens och senoterapier. Cancer 12 (8): 2134.
- Wang, Y. & He, Y. & Rayman, M. & Zhang, J. (2021). Prospektiv selektiv mekanism för nya senolytiska medel som härrör från flavonoider. Journal of Agricultural and Food Chemistry 69 (42): 12418–12423.
- Wiciński, M. et al (2023). Naturliga fytokemikalier som SIRT-aktivatorer - fokus på potentiella biokemiska mekanismer. Näringsämnen 15 (16): 3578.
- Afroze, N. et al (2022). Fisetin förhindrar cellproliferation, inducerar apoptos, lindrar oxidativ stress och inflammation i mänskliga cancerceller, HeLa. Internationell tidskrift för molekylära vetenskaper 23 (3): 1707.
- Roy, T. et al (2023). Dubbel inriktning av mTOR/IL-17A och autofagi genom fisetin lindrar psoriasisliknande hudinflammation. Gränser inom immunologi 13: 1075804.
- Samanta, S. et al (2022). De neuroprotektiva effekterna av fisetin, en naturlig flavonoid i neurodegenerativa sjukdomar: Fokus på rollen som oxidativ stress. Gränser inom farmakologi 13: 1015835.
- Singh, S. & Singh, A. & Garg, G. & Rizvi, S. I. (2018). Fisetin som en mimetisk kalorirestriktion skyddar råtthjärnan mot åldrande inducerad oxidativ stress, apoptos och neurodegeneration. Biovetenskap 193: 171–179.
- Verdoorn, B. et al (2021). Fisetin för COVID-19 i kvalificerade vårdinrättningar: Senolytiska prövningar i COVID-eran. Journal of the American Geriatrics Society 69 (11): 3023–3033.
- Kirkland, J. (2024). Lindring genom Fisetin av skörhet, inflammation och relaterade åtgärder hos äldre kvinnor (AFFIRM). Kliniska prövningar.gov ID: NCT03430037.
- Chirumbolo, S. (2010). Rollen för quercetin, flavonoler och flavoner i moduleringen av inflammatorisk cellfunktion. Inflammation & allergi - mål för läkemedel 9 (4): 263–285.
- Chirumbolo, S. (2011). Quercetin som ett potentiellt antiallergiskt läkemedel: vilka perspektiv? Iran Journal of Allergy Asthma and Immunology 10 (2): 139–140.
- Sagit, M. et al (2017). Effektivitet av quercetin i en experimentell råttmodell av allergisk rinit. European Archives of Oto-Rhino-Laryngology 274 (8): 3087–3095.
- Li, Y. et al (2016). Quercetin, Inflammation och Immunitet. Näringsämnen 8 (3): 167.
- Costa, L. & Garrick, J. & Roquè, P. & Pellacani, C. (2016). Mekanismer för neuroskydd genom quercetin: Motverkar oxidativ stress och mycket mer. Oxidativ medicin och cellulär livslängd 2016: 2986796.
- Cui, Z. et al. (2022). Terapeutisk tillämpning av quercetin i åldersrelaterade sjukdomar: SIRT1 som en potentiell mekanism. Gränser inom immunologi 13: 943321.
- Suraweera, T. & Rupasinghe, H. & Dellaire, G. & Xu, Z. (2020). Reglering av Nrf2/ARE-vägen genom flavonoider i kosten: En vän eller fiende för cancerhantering? Antioxidanter 9: 973.
- Salehi, B. et al (2019). Den terapeutiska potentialen hos apigenin. Internationell tidskrift för molekylära vetenskaper 20 (6): 1305.
- Paredes-Gonzalez, X. et al (2015). Induktion av NRF2-medierat genuttryck av fytokemiska flavoner apigenin och luteolin i kosten. Biofarmaci och läkemedelsdisposition 36 (7): 440–451.
- Ginwala, R. & Bhavsar, R. & Chigbu, D. & Jain, P. & Khan, Z. (2019). Flavonoidernas potentiella roll vid behandling av kroniska inflammatoriska sjukdomar med särskilt fokus på apigenins antiinflammatoriska aktivitet. Antioxidanter 8 (2): 35.
- Shukla, S. & Gupta, S. (2010). Apigenin: en lovande molekyl för förebyggande av cancer. Farmaceutisk forskning 27: 962–978.
- Sung, B. & Chung, H. & Kim, N. (2016). Apigenins roll i förebyggande av cancer via induktion av apoptos och autofagi. Journal of Cancer Prevention 21 (4): 216-226.
- Pan, H. & Finkel, T. (2017). Viktiga proteiner och vägar som reglerar livslängden. Tidskrift för biologisk kemi 292 (16): 6452–6460.
- Shukla, S. & Gupta, S. (2009). Apigenin undertrycker insulinliknande tillväxtfaktor I-receptorsignalering i mänsklig prostatacancer: En in vitro- och in vivo-studie. Molekylär carcinogenes 48 (3): 243–252.
- Escande, C. et al (2013). Flavonoid apigenin är en hämmare av NAD + ase CD38: implikationer för cellulär NAD + metabolism, proteinacetylering och behandling av metaboliskt syndrom. Diabetes 62 (4): 1084–1093.
- Lim, H. & Park, H. & Kim, H. (2015). Effekter av flavonoider på senescensassocierad sekretorisk fenotypbildning från bleomycininducerad senescens i BJ-fibroblaster. Biokemisk farmakologi 96 (4): 337–348.
- Salehi, B. et al (2019). Den terapeutiska potentialen hos apigenin. Internationell tidskrift för molekylära vetenskaper 20 (6): 1305.