NAD+ on koentsyymi, jota esiintyy kaikissa elävissä soluissa ja joka on välttämätön elimistön perustoiminnoille. NAD+-tasot laskevat ikääntyessämme, minkä uskotaan olevan osasyynä ikääntymisprosessiin.
Nikotiiniamidi-adeniinidinukleotidi (NAD+/NADH).
NAD löydettiin ensimmäisen kerran hiivan käymisen aikana. Sen löytämisen jälkeen on havaittu, että NAD (nikotiiniamidiadeniinidinukleotidi) on tärkeä kofaktori, joka osallistuu lähes kaikkiin solureaktioihin. Näihin kuuluvat DNA:n korjaus, immuunijärjestelmän toiminta, ATP:n tuotanto ja vuorokausikellon toiminta. NAD+ edistää energiantuotantoa ja mahdollistaa solujen asianmukaisen toiminnan. NAD+-tasojen säätelyhäiriöt on yhdistetty aineenvaihduntasairauksiin ja ikääntymiseen liittyviin sairauksiin, kuten neurodegeneraatioon, puutteellisiin immuunivasteisiin ja syöpään..
NAD:lla on kaksi muotoa - NAD+ ja NADH, jotka molemmat hallitsevat elektroninsiirtoreaktioita.:
- NAD+ on hapettava aine, joka poimii elektroneja muista molekyyleistä ja pelkistyy siten.
- NADH on pelkistävä aine, joka muodostuu pelkistyneestä NAD+:sta ja jota käytetään sitten luovuttamaan elektroneja muille molekyyleille, jolloin siitä tulee jälleen NAD+.
- NADH:n elektronit voivat varastoida energiaa, joka muunnetaan ATP:ksi mitokondriossa hapettuvaksi fosforylaatioksi kutsutussa prosessissa mitokondriossa (ks. biohakkeriKäsikirjan harjoituksia käsittelevästä luvusta. lisätietoja)
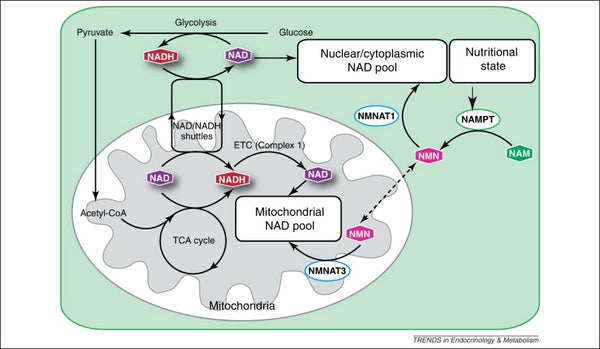
Kuva: Mitokondrioiden NAD-varaston ylläpito.
Lähde: Stein, L. & Imai, S. (2012). NAD-aineenvaihdunnan dynaaminen säätely mitokondrioissa. Endokrinologian ja aineenvaihdunnan suuntaukset. 23 (9): 420–428.
Johdanto NAD+:een
Ihannetapauksessa NAD+ on homeostaattisessa biosynteesin, kulutuksen, kierrätyksen ja hajoamisen tilassa sekä solu- että systeemitasolla. Ihmisen solut voivat syntetisoida NAD+ de novo tryptofaanista kynureniinireitin kautta tai nikotiinihaposta (NA) Preiss-Handler-reitin kautta. Kuitenkin, suurin osa NAD+:sta kierrätetään nikotiiniamidista (NAM), NA:sta, nikotiiniamidiribosidista (NR) ja nikotiiniamidimononukleotidista (NMN) pelastusreitillä solujen NAD+-tasojen ylläpitämiseksi. NAD+ voidaan pelkistää NADH:ksi erilaisissa aineenvaihduntaprosesseissa, kuten glykolyysissä, rasvahappojen hapettumisessa ja Krebsin syklissä.
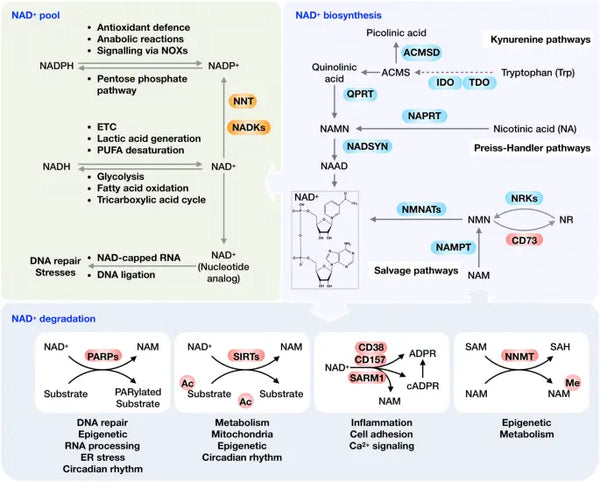
Kuva: Yleiskatsaus NAD+-aineenvaihduntaan ja sen fysiologiseen toimintaan.
Lähde: Xie, N. et al. (2020). NAD+-aineenvaihdunta: patofysiologiset mekanismit ja terapeuttiset mahdollisuudet. Signaalinsiirto ja kohdennettu hoito 5 (1): 1–37.
Koska NAD+ on erilaisten perustavanlaatuisten makromolekyylien kannalta tärkeä liitännäissubstraatti, NAD+:aa kuluttavat entsyymit voivat pilkkoa sitä. Näitä ovat muun muassa PARP:t, sirtuiinit, CD38 ja SARM1, jolloin syntyy NAM ja ADP-riboosi (ks. kuva). Normaaleissa homeostaattisissa olosuhteissa CD38:n ilmentyminen on vähäistä, kun taas CD38:n ilmentyminen on vähäistä. CD38:n lisääntyvä ilmentyminen ikääntymisen myötä on keskeisessä asemassa ikään liittyvässä NAD+:n vähenemisessä.. Tätä käsitystä vahvistaa havainto, että PARP1:n ja CD38:n esto lisää tehokkaasti NAD+:n kokonaissaatavuutta, mikä johtaa SIRT1:n aktivoitumiseen..
NAD+-tasojen väheneminen liittyy viimeaikaisen tieteen perusteella ikääntymiseen. On yleistä, että NAD+-tasot laskevat alle puoleen 60 ikävuoden jälkeen verrattuna parikymppisten tasoihin. Suuri kysymys on, miksi NAD+-tasot ylipäätään laskevat. Tästä on esitetty pari teoriaa, mutta viimeisin ja eniten tukea saanut teoria on, että NAD+-tasot laskevat iän myötä, koska NAD:ää kuluttavan entsyymin CD38:n ylitoiminta tuhoaa sitä.. Alhaisen NAD+-tilan tiedetään myös estää elimistön immuunijärjestelmää ja luonnollisia puolustusmekanismeja..
CD38, joka tunnetaan myös nimellä syklinen ADP-riboosihydrolaasi, on glykoproteiini, jota esiintyy monien immuunisolujen (erityisesti valkosolujen), kuten B-lymfosyyttien, luonnollisten tappajasolujen, CD4⁺- ja CD8-solujen pinnalla. Yleensä tulehduksen lisääntyminen lisää CD38:n ilmentymistä, mikä sitten kuluttaa NAD+:a. Siksi, matala-asteisen tulehduksen ja tulehduksen hallinta yleensä on paras tapa minimoida ikääntymisestä johtuva NAD+:n menetys..
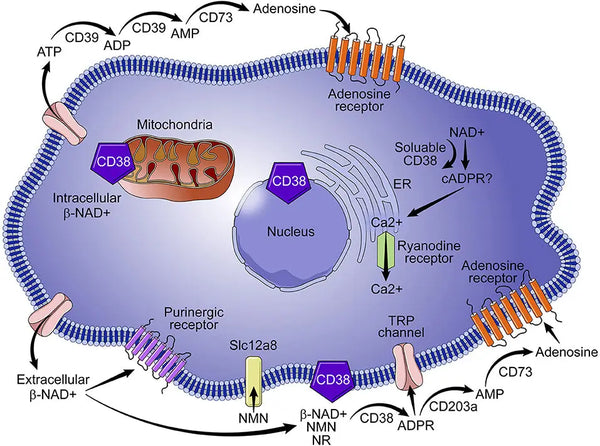
Kuva: CD38:n rooli NAD+-aineenvaihdunnassa.
Lähde: Hogan, K. & Chini, C. & Chini, E. (2019). Monipuolinen ektoentsyymi CD38: roolit immunomodulaatiossa, syövässä, ikääntymisessä ja aineenvaihduntasairauksissa. Frontiers in Immunology 10: 1187.
NAD+ lievittää virus- ja bakteeri-infektioiden aiheuttamia oksidatiivisia vaurioita
Virusinfektiot ja infektiot yleensä aiheuttavat hapetusstressiä isäntäsoluissa. (esim. ihmisen solut). Näin ollen oksidatiivista stressiä pidetään virusinfektioiden patogeenisena tekijänä. Virusinfektion aiheuttama lisääntynyt solujen reaktiivisten happilajien määrä aiheuttaa esimerkiksi DNA-vaurioita, geenimutaatioita, solukuolemaa, viruksen DNA:n integroitumista ja kasvainten syntyä. Oksidatiivisen stressin aiheuttamien DNA-vaurioiden korjaamiseksi tarvitaan suuri määrä NAD+:a, jota kohonneet PARP:t kuluttavat vastauksena virusinfektioon.
Sirtuiinit ovat toinen NAD+:aa kuluttavien entsyymien luokka, jotka ovat olleet laaja-alaisia antiviraalisia ominaisuuksia erilaisiin viruksiin (mukaan lukien HIV-1, HCMB, H1N1 ja HCV).. CD38 on kolmas NAD+:aa kuluttava entsyymi, joka yliekspressoituu vasteena useisiin virusinfektioihin. CD38:n puutos johtaa lisääntyneeseen alttiuteen useille patogeeneille.
Bakteeri-infektiot aiheuttavat myös solunsisäisten reaktiivisten happilajien (ROS) nopeaa tuotantoa. joko NADPH-oksidaasien (NOX) tai mitokondrioiden toimesta, jotka ovat välttämättömiä, jotta makrofagit voivat poistaa bakteerit. NAD+/NADH vaikuttaa bakteerien tuhoamiseen edistämällä ROS:n muodostumista, tulehdusta edistävää vastetta ja infektion vastaista autofagiaa. Tämä hyödyllinen ja luonnollinen aineenvaihduntaprosessi tarvitsee hyvin toimivaa NAD+-aineenvaihduntaa ja optimaalisia NAD+-tasoja toimiakseen oikein. ROS:n eliminointi johtaa puutteelliseen bakterisidiseen (bakteereja tappavaan) aktiivisuuteen, jolloin bakteerit voivat selviytyä ja kolonisoitua toistuvasti eri kudospaikkoihin..
Tämä on syy siihen, miksi liian monien antioksidanttien käyttö koko ajan ei ole hyödyllistä immuunijärjestelmälle. Optimaalisen homeostaasin kannalta keskeistä on tasapaino hapetusstressin ja antioksidanttikapasiteetin välillä.
Kehitteillä oleva näyttö tukee hypoteesia, jonka mukaan CD38:lla ja CD38/NAD+-akselin kontrolloimilla tuotteilla voi olla merkittävä rooli SARS-CoV-2-infektion patogeneesissä.. CD38:n liiallinen ilmentyminen COVID-19:ssä aiheuttaa solukuolemaa pääasiassa NAD+:n ehtymisen kautta.. NAD+:n esiasteiden (NR, NAM ja NMN) antaminen suun kautta näyttää olevan tehokkain tapa täydentää NAD+-tasoja (ks. myöhemmin). Näistä NAD+:n esiasteista NR:llä (täydennettynä 1 gramma päivässä) on tulehdusta ehkäiseviä vaikutuksia eri tautitiloissa. Nykyinen tieteellinen näyttö näyttää vahvistavan, että NAD+:n biosynteesin ja kulutuksen avaintapahtumilla on merkittävä rooli virusperäisessä immuunivasteessa.. NAD+-tasojen lisääminen biosynteettisiä reittejä moduloimalla. tai vähentämällä NAD+:n kulutusta voi auttaa hillitä hyperimmuunivastetta SARS-CoV-2-infektioon..
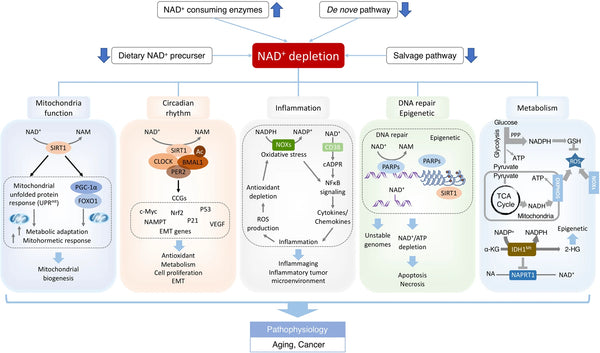
Kuva: NAD+:n puutteet ikääntymiseen liittyvissä toimintahäiriöissä ja syövässä.
Lähde: Xie, N. et al. (2020). NAD+-aineenvaihdunta: patofysiologiset mekanismit ja terapeuttiset mahdollisuudet. Signaalinsiirto ja kohdennettu hoito 5 (1): 1–37.
Elämäntapatekijät, jotka vähentävät NAD+-tasoja:
- Sirkadiaanisen rytmin epäsuhta
- Krooninen tulehdus ja oksidatiivinen stressi
- Jatkuva kaloriylijäämä (syö koko ajan liikaa) - korkeampi NADH, matalampi NAD+.
- Kohonneet verensokeri- ja insuliinitasot
- Krooninen alkoholin käyttö
NAD+:n puutteen mahdolliset seuraukset:
- Heikentynyt immuunijärjestelmän toiminta
- Nopeutunut ikääntyminen
- Mitokondrioiden toimintahäiriöt
- häiriintynyt vuorokausikello (ikääntymisen myötä)
- Lisääntynyt karsinogeneesi ja syöpäriski.
- Lisääntynyt insuliiniresistenssin ja diabeteksen kehittymisen riski.
- lisääntynyt lihavuuden riski
- Lisääntynyt riski sairastua ei-alkoholiperäiseen rasvamaksasairauteen.
- Lisääntynyt riski sairastua hermoston rappeutumishäiriöihin.
- Lisääntynyt sydän- ja munuaisten vajaatoiminnan riski
Parhaat tavat lisätä NAD+-tasoja kehossa:
Yleensä solunsisäiset NAD+-tasot pysyvät solutyypistä tai kudoksesta riippuen 0,2-0,5 mM:n välillä. NAD+:n pitoisuus ja jakautuminen voi kuitenkin vaihdella erilaisten fysiologisten ärsykkeiden ja solustressien seurauksena.
- Harjoittele säännöllistä (ajoittaista) paastoa ja kalorimäärän rajoittamista. (Lue lisää täältä)
- Aktivoi elimistön ketogeneesi ja pidä säännölliset glukoosin rajoitusjaksot.
- Harjoittele säännöllisesti
- Harjoittele lämmönvaihtelua (lue lisää täältä)
- Parhaita NAD+:n esiasteiden elintarvikelähteitä ovat mm:
- Raaka- ja fermentoidut maitotuotteet (sisältävät runsaasti NR:ää).
- Rasvainen kala, kuten lohi, sardiini, taimen ja makrilli (sisältää runsaasti niasiinia).
- Poron-, naudan- ja kananmaksa (sisältää runsaasti niasiinia).
- Sianliha ja kalkkuna (sisältävät runsaasti tryptofaania ja niasiinia).
- Naudanliha (sisältää runsaasti niasiinia)
- Täydennä NAD+:n esiasteilla
- Nikotiiniamidi-ribosidi (NR): optimiannos 300 mg päivässä.
- Nikotinamidimononukleotidi (NMN): optimiannos 250-500 mg päivässä.
- Liposomaalinen annos on noin 10 kertaa pienempi.
- Käytä yhdessä trimetyyliglysiinin (TMG) kanssa optimaalisen metylaatioprosessin saavuttamiseksi.
- Niasiiniamidi (NAM): optimaalinen annos 250-500 mg päivässä.
- Nikotiinihappo (NA): optimaalinen annos 250-500 mg päivässä.
NAD+:n esiasteiden, erityisesti NR:n ja NMN:n, jatkuvan täydentämisen turvallisuudesta ei ole pitkäaikaista tietoa. Liian korkeat NAD+-tasot voivat myös aiheuttaa häiriöitä NAD+/NADH-homeostaasissa. Näitä ovat muun muassa vuorokausirytmin epäsuhta ja hiirillä tehtyjen tutkimusten perusteellaunijakson häiriöt sekä häiriintynyt nälkä ja ruokahalu.. Tämän perusteella voi olla ihanteellista ottaa NAD+-esiasteita aamulla.
Suositellut lisäravinteet:
Purovitalis Liposomaalinen NMN.
Korkean NAD+-pitoisuuden fysiologiset hyödyt elimistössä:
- Optimaalinen mitokondrioiden toiminta
- Ratkaiseva biokemiallinen tekijä energiantuotannossa ja lihasten toiminnassa
- Optimaalinen aivotoiminta ja neurodegeneraation ehkäisy
- Optimaalinen uni-valverytmi ja luonnollisen vuorokausirytmin ylläpitäminen.
- Suojaus oksidatiiviselta stressiltä ja tulehdus
- Solujen selviytyminen ja hapen tuotanto
- Hidastettu ikääntyminen ja pidempi elinikä ja terveysväli. kautta mitofagian ja DNA:n korjaamisen kautta (hiirillä tehtyjen tutkimusten perusteella).
- Sydänsairauksien riskin väheneminen kumoamalla ikään liittyviä valtimoiden toimintahäiriöitä ja parantunut yleinen sydänterveys (hiirillä tehtyjen tutkimusten perusteella)
- Vähentää ihon ikääntymistä
///





