Lo studio della resilienza attraverso la lente della genetica è un campo di interesse in espansione, che spesso si interseca con le discipline della psicologia, della neurobiologia e della genomica. Sebbene il concetto di resilienza - la capacità di riprendersi o adattarsi alle avversità o allo stress - sia sfaccettato e influenzato da una complessa interazione di fattori genetici, ambientali e psicologici, sono stati sviluppati specifici test del DNA per far luce sulle componenti genetiche di questa caratteristica.
Introduzione
I geni sono segmenti di DNA che contengono le istruzioni necessarie all'organismo per produrre ciascuna delle migliaia di proteine necessarie alla vita. Ogni gene comprende migliaia di combinazioni di "lettere" (chiamate basi) che costituiscono il codice genetico. Il codice fornisce le istruzioni per produrre le proteine necessarie per il corretto sviluppo e funzionamento.(1)
Le variazioni genetiche possono influenzare l'espressione di un gene, influenzando così i processi metabolici che sono importanti per mantenere la salute delle cellule e il modo in cui rispondiamo agli interventi ambientali come la dieta, lo stile di vita, gli integratori e i farmaci.
La conoscenza di queste variazioni genetiche offre una visione impareggiabile dei sistemi biologici, consentendo agli operatori sanitari di raccomandare interventi precisi per aiutare a raggiungere i propri obiettivi e ottenere una salute ottimale.
Comprendere i marcatori genetici della resilienza
La resilienza-la capacità di riprendersi o di adattarsi facilmente alle avversità o ai cambiamenti- è sempre più vista attraverso la genetica. Esaminando i marcatori genetici, ricercatori e medici mirano a scoprire le basi biologiche che potrebbero spiegare perché alcuni individui si riprendono dallo stress e dai traumi in modo più efficace di altri.(2) Questo fiorente campo di indagine si è concentrato sui test del DNA relativi alla resilienza, che esaminano i marcatori genetici potenzialmente responsabili delle differenze nelle risposte individuali allo stress.
Al centro di questa ricerca ci sono i sistemi endocrino e nervoso. (in particolare il sistema nervoso autonomo), centrali nella risposta dell'organismo allo stress. L'asse ipotalamo-ipofisi-surrene (HPA), in particolare, è un'area centrale di interesse, poiché svolge un ruolo critico nella regolazione del meccanismo di risposta allo stress dell'organismo. Questa complessa rete di interazioni tra l'ipotalamo, l'ipofisi e le ghiandole surrenali orchestra la produzione e la regolazione degli ormoni chiave dello stress, come il cortisolo.
Il cortisolo ha effetti di vasta portata su molte funzioni corporee e viene rilasciato in risposta allo stress e a una bassa concentrazione di glucosio nel sangue. In circostanze normali, il cortisolo aiuta a ripristinare l'omeostasi dopo eventi stressanti. Tuttavia, le variazioni genetiche che influenzano l'asse HPA possono portare a differenze nel modo in cui il cortisolo viene prodotto, regolato e eliminato dall'organismo. Queste variazioni genetiche possono influenzare la resilienza fisiologica di un individuo, ovvero la sua capacità di mantenere o ripristinare rapidamente la salute psicofisica dopo le avversità.(3)
Test del DNA per la resilienza studiano le varianti geniche associate ai recettori degli ormoni dello stress, alle proteine coinvolte nelle vie degli ormoni dello stress e agli enzimi che metabolizzano questi ormoni. Ad esempio, una variante del gene FKBP5, coinvolto nella regolazione della sensibilità del recettore dei glucocorticoidi attraverso il quale il cortisolo esercita i suoi effetti, potrebbe modificare la risposta allo stress di un individuo e potenzialmente la sua suscettibilità ai disturbi legati allo stress. Per ampliare ulteriormente la portata, sono sotto i riflettori anche i geni che codificano per i neurotrasmettitori, i messaggeri chimici del cervello che contribuiscono alla regolazione dell'umore e alla cognizione. Tra questi vi sono geni come il COMT, che è determinante nella scomposizione della dopamina, un neurotrasmettitore associato al piacere e ai sistemi di ricompensa.(4)
Inoltre, infiammazione è un processo biologico strettamente collegato allo stress e ai disturbi dell'umore. L'infiammazione cronica, che può essere influenzata da variazioni genetiche, può influenzare la funzione cerebrale e il comportamento.(5) Pertanto, i test genetici potrebbero anche cercare di identificare varianti nei geni delle citochine pro-infiammatorie, come IL-6 e TNF, che potrebbero predisporre gli individui a risposte infiammatorie prolungate e influenzare la loro resilienza mentale.
La comprensione di questi marcatori genetici è la chiave di volta per interventi personalizzati. Identificando le predisposizioni genetiche, gli individui possono adottare misure proattive per rafforzare la loro resilienza attraverso modifiche dello stile di vita, strategie psicologiche e trattamenti medici personalizzati in base alla loro composizione genetica unica. Questo approccio esemplifica il passaggio alla medicina di precisione, dove il modello unico lascia il posto a cure più personalizzate.
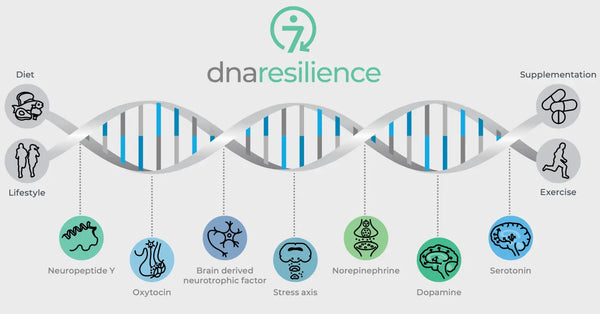
Immagine: Le sette vie molecolari della resilienza.
Tipi di test del DNA per la resilienza
1) Geni della risposta allo stress
I geni della risposta allo stress sono componenti fondamentali del sistema di gestione e risposta dell'organismo ai fattori di stress. Codificano proteine che regolano vari processi fisiologici, tra cui il rilascio e l'azione del cortisolo, un ormone fondamentale nella risposta allo stress.
CRHR1 (recettore 1 dell'ormone di rilascio della corticotropina)
CRHR1 codifica un recettore per l'ormone di rilascio della corticotropina (CRH), un ormone centrale che avvia la risposta allo stress. Quando il CRH si lega al CRHR1, stimola la produzione e il rilascio dell'ormone adrenocorticotropo (ACTH), che induce le ghiandole surrenali a produrre cortisolo. Le varianti del gene CRHR1 possono influenzare la sensibilità di questo recettore al CRH, alterando la risposta complessiva allo stress. Per esempio, alcuni polimorfismi possono portare a un'accentuata risposta allo stress, che potrebbe contribuire all'ansia o alla depressione. Al contrario, altri possono smorzare la risposta, influenzando la capacità di gestire lo stress acuto.(6-7)
FKBP5 (FK506 Binding Protein 5)
Il gene FKBP5 svolge un ruolo nella regolazione della sensibilità del recettore dei glucocorticoidi, che è il recettore attraverso il quale il cortisolo esercita i suoi effetti. Polimorfismi specifici in FKBP5 sono stati collegati a un'alterata inibizione del feedback dell'asse HPA e a risposte differenziate ai glucocorticoidi. Ad esempio, alcune varianti di FKBP5 possono ridurre l'affinità del recettore dei glucocorticoidi per il cortisolo, portando potenzialmente a un'alterata risposta allo stress e a un aumento del rischio di disturbi psichiatrici legati allo stress, come il PTSD o la depressione maggiore.(8-9)
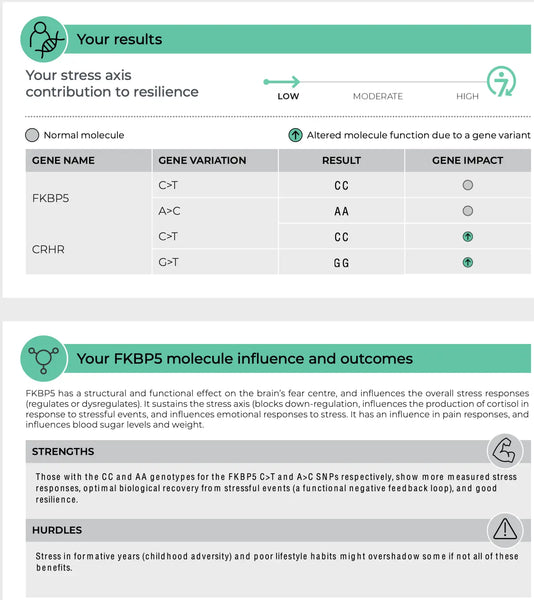
Immagine: Una pagina di esempio del sito DNA Resilience.
NR3C1 (Sottofamiglia 3 dei recettori nucleari, gruppo C, membro 1)
NR3C1 codifica il recettore dei glucocorticoidi. Le variazioni di questo gene possono influenzare il modo in cui l'organismo reagisce al cortisolo. Polimorfismi specifici in NR3C1 possono influenzare la sensibilità o la densità dei recettori dei glucocorticoidi, incidendo sull'efficacia con cui il cortisolo può svolgere le sue funzioni. Questo può portare a una serie di risposte, da una risposta allo stress attenuata che può impedire a un individuo di reagire adeguatamente ai fattori di stress a una risposta esagerata che può provocare sintomi di stress cronico e persino depressione.(10-12)
I risultati dei test genetici sulla risposta allo stress possono fornire indicazioni sulla predisposizione di un individuo a problemi di salute legati allo stress. Per esempio:
-
Risposta allo stress accentuata: Gli individui con varianti specifiche potrebbero essere più reattivi allo stress e sperimentare livelli di cortisolo più elevati durante gli eventi stressanti.
-
Riduzione della risposta allo stress: Al contrario, alcuni individui potrebbero avere una risposta allo stress attenuata, che potrebbe essere protettiva in situazioni di stress acuto, ma potrebbe anche ostacolare l'attivazione dei meccanismi fisiologici necessari in risposta alle sfide.
2) Spiegazioni sui test di funzionalità dei neurotrasmettitori
I test di funzionalità dei neurotrasmettitori sono progettati per studiare i fattori genetici che influenzano il modo in cui i neurotrasmettitori vengono sintetizzati, rilasciati e scomposti nel cervello. Poiché i neurotrasmettitori sono messaggeri chimici che regolano l'umore, la cognizione e le risposte allo stress, le variazioni nei geni correlati a queste sostanze possono avere implicazioni significative per la capacità di recupero psicologico e la salute mentale complessiva di un individuo.
L'esplorazione della funzione dei neurotrasmettitori nel contesto della resilienza e della risposta allo stress va oltre le catecolamine come la dopamina. Include un più ampio spettro di sistemi di neurotrasmettitori coinvolti nella regolazione dell'umore, nella vigilanza e nella funzione cognitiva. Diversi geni sono coinvolti nella sintesi, segnalazione e degradazione di questi neurotrasmettitori, tra cui la dopamina beta-idrossilasi (DBH), i recettori della dopamina (DRD2, DRD4) e vari geni legati alla serotonina.(13)
COMT (catecol-O-metiltransferasi)
Il gene COMT è uno dei più studiati per quanto riguarda la funzione dei neurotrasmettitori. Codifica un enzima che scompone le catecolamine, come la dopamina, l'epinefrina e la noradrenalina, neurotrasmettitori fondamentali per la risposta allo stress, la cognizione e la regolazione delle emozioni.
Esistono noti polimorfismi nel gene COMT, come la variante Val158Met. Questa variante può influenzare il livello di attività dell'enzima in diversi modi:(14-15)
- Forma ad alta attività (variante Val): Questa forma dell'enzima scompone la dopamina a un ritmo più veloce, il che può portare a livelli più bassi di dopamina nella corteccia prefrontale, una regione del cervello coinvolta nella funzione esecutiva e nel processo decisionale. I soggetti con questa variante possono avere prestazioni migliori in compiti in condizioni stabili, ma potrebbero essere più suscettibili al declino cognitivo in condizioni di stress a causa della minore disponibilità di dopamina.
- Forma a bassa attività (variante Met): Al contrario, questa forma dell'enzima COMT metabolizza la dopamina più lentamente, con conseguente aumento dei livelli di dopamina nel cervello. Ciò può migliorare le funzioni cognitive sotto stress, ma può anche aumentare il rischio di psicopatologie legate allo stress, come i disturbi d'ansia, poiché il cervello è potenzialmente sovrastimolato dall'eccesso di dopamina.
Dopamina Beta-Idrossilasi (DBH)
La DBH è un enzima che converte la dopamina in noradrenalina, un neurotrasmettitore coinvolto nella risposta "lotta o fuga". Le variazioni genetiche del gene DBH possono influire sull'attività dell'enzima, influenzando i livelli di dopamina e noradrenalina nel cervello e nel sistema nervoso periferico.(16-18)
- Bassa attività: Le varianti associate a una minore attività del DBH possono portare a livelli più elevati di dopamina e a livelli ridotti di noradrenalina, che possono influire su funzioni cognitive come l'attenzione e il processo decisionale e influenzare il modo in cui un individuo risponde allo stress.
- Attività elevata: Al contrario, le varianti che determinano un'attività DBH più elevata possono ridurre i livelli di dopamina e aumentare quelli di noradrenalina, con un potenziale impatto sulla reattività allo stress e sull'ansia.
Recettori della dopamina (DRD2 e DRD4)
DRD2 e DRD4 sono geni che codificano rispettivamente i recettori della dopamina D2 e D4. Questi recettori fanno parte del sistema della dopamina che regola numerose funzioni, tra cui l'umore, la ricompensa e il controllo motorio.(19-20)
- DRD2: Le varianti del gene DRD2 possono influenzare la densità e l'affinità di legame dei recettori D2. Ciò può influenzare la vulnerabilità allo stress e l'efficacia degli stimoli legati alla ricompensa, con potenziali implicazioni per condizioni come la dipendenza e la depressione.
- DRD4: Il gene DRD4 è noto per un numero variabile di ripetizioni in tandem (VNTR) nella regione codificante. Specifiche ripetizioni sono associate a tratti come la ricerca di novità e il rischio di disturbi dell'attenzione. Questo polimorfismo può influenzare l'efficienza della segnalazione sinaptica della dopamina ed è stato studiato nel contesto della resilienza comportamentale e psicologica.
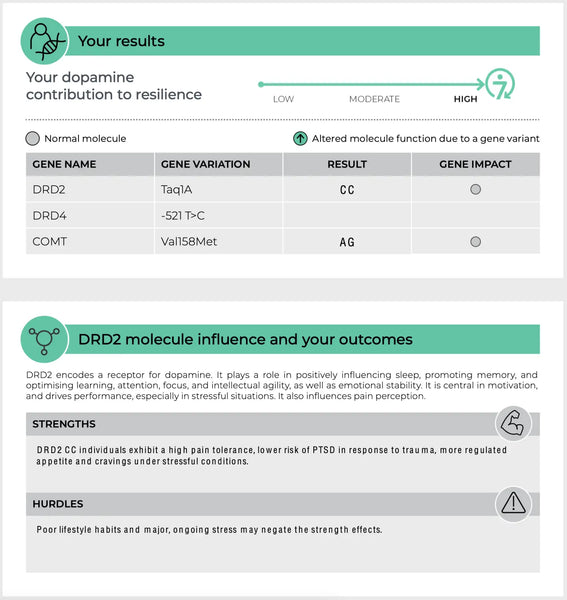
Immagine: Una pagina di esempio del sito test di resilienza del DNA.
Variazioni del gene della serotonina
La serotonina è un altro neurotrasmettitore cruciale nella regolazione dell'umore, dell'appetito e del sonno, tutti fattori che possono essere influenzati dallo stress. Diversi geni coinvolti nella segnalazione della serotonina sono interessanti:
- 5-HTT (SLC6A4): Questo gene codifica il trasportatore della serotonina, responsabile della ricaptazione della serotonina dalla fessura sinaptica. Il polimorfismo 5-HTTLPR nella regione promotrice di questo gene è stato studiato per la sua associazione con la sensibilità allo stress e i disturbi dell'umore.(21)
- MAOA: Il gene della monoamino ossidasi A è responsabile della scissione della serotonina. Le variazioni di questo gene possono influenzare i livelli di serotonina e sono state associate a tratti comportamentali e alla suscettibilità allo stress.(22)
- TPH2: La triptofano idrossilasi-2 è un enzima fondamentale per la sintesi della serotonina nel cervello. Le variazioni genetiche nella TPH2 possono influenzare la produzione di serotonina, incidendo potenzialmente sulla regolazione emotiva e sulla risposta allo stress.(23)
L'interpretazione dei risultati di questi test può essere complessa. Ad esempio, una variante associata a un rischio maggiore di condizioni legate allo stress non significa necessariamente che un individuo svilupperà tali condizioni, ma può suggerire una maggiore vulnerabilità. Allo stesso modo, il possesso di una variante "resilienza" non garantisce una resistenza inattaccabile allo stress, poiché i fattori ambientali e le scelte di vita giocano un ruolo fondamentale.
3) L'infiammazione e il suo impatto sul cervello
L'infiammazione cronica può essere dannosa per la salute del cervello. Si ritiene che contribuisca allo sviluppo e alla progressione delle malattie neurodegenerative e che possa influenzare la risposta del cervello allo stress, che è strettamente legata alla resilienza. Le citochine pro-infiammatorie, come l'interleuchina-6 (IL-6) e il fattore di necrosi tumorale (TNF), possono attraversare la barriera emato-encefalica e interagire con le vie che regolano l'umore, la motivazione e la vigilanza.(24)
Varianti geniche associate all'infiammazione
IL-6 (Interleuchina-6)
L'IL-6 è una citochina che svolge un ruolo nella risposta infiammatoria ed è coinvolta in varie funzioni biologiche, tra cui la risposta immunitaria, l'emopoiesi e il metabolismo osseo. Nel contesto dello stress e della resilienza, l'IL-6 è correlata a quanto segue:(25-26)
- Livelli elevati di IL-6 sono stati associati a un maggior rischio di sviluppare depressione e altri disturbi dell'umore.
- Specifiche varianti genetiche del gene dell'IL-6 possono portare a una maggiore espressione dell'IL-6, potenzialmente esacerbando la risposta infiammatoria e alterando la capacità del cervello di far fronte allo stress.
TNF (Fattore di necrosi tumorale)
Il TNF è un'altra citochina coinvolta nell'infiammazione sistemica. Ha diversi ruoli, tra cui la regolazione delle cellule immunitarie e l'induzione di febbre, apoptosi e infiammazione.(27)
- La sovraespressione del TNF è stata collegata a diverse malattie croniche, tra cui l'artrite reumatoide, le malattie infiammatorie intestinali e la psoriasi, oltre che allo stress psicologico e alla depressione.
- Le varianti del gene TNF possono influenzare il livello di produzione di TNF, con implicazioni dirette sui processi infiammatori dell'organismo e del cervello.
4) Regolatori neurobiologici e fattori di resilienza
Le variazioni genetiche in regolatori neurobiologici cruciali regolano anche la resilienza allo stress. Questi includono l'ossitocina, il fattore neurotrofico derivato dal cervello (BDNF) e il neuropeptide Y (NPY). L'ossitocina svolge un ruolo nella regolazione dei comportamenti sociali e delle risposte allo stress. Il BDNF è fondamentale per mantenere la neuroplasticità e le funzioni cognitive sotto stress e l'NPY modula l'ansia e la risposta fisiologica allo stress. Queste molecole hanno un impatto collettivo sui nostri circuiti neurali e sulla nostra resilienza psicologica, fornendo indicazioni sulle differenze individuali nella resilienza allo stress e potenziali vie per strategie di biohacking personalizzate.
Ossitocina
L'ossitocina è spesso chiamata "ormone dell'amore" per il suo ruolo nel legame sociale, nei comportamenti materni e nell'intimità. Esercita anche effetti ansiolitici e influenza la cognizione sociale e il comportamento.
- Influenza genetica: Le variazioni nel gene del recettore dell'ossitocina (OXTR) sono state associate alla regolazione emotiva, al comportamento sociale e alla reattività allo stress. Polimorfismi specifici nell'OXTR possono influenzare l'efficienza di legame e i livelli di espressione dei recettori dell'ossitocina, che possono influire sulla capacità di un individuo di gestire lo stress e di formare relazioni sociali.(28)
- Implicazioni: Nel contesto dei test di resilienza, la valutazione delle varianti di OXTR può fornire indicazioni sulla predisposizione all'ansia sociale, sui livelli di empatia e sulla potenziale resilienza di un individuo di fronte allo stress, in particolare quello che coinvolge le dinamiche sociali.(29)
Fattore neurotrofico derivato dal cervello (BDNF)
Il BDNF è una proteina cruciale coinvolta nella neuroplasticità, la capacità del cervello di riorganizzarsi e formare nuove connessioni neurali nel corso della vita. È fondamentale per l'apprendimento, la memoria e la rigenerazione dei neuroni.(30)
- Variazioni genetiche: La variante Val66Met del gene BDNF è uno dei polimorfismi più studiati. L'allele Met è stato associato a una ridotta secrezione di BDNF dipendente dall'attività, che potrebbe influire sulla funzione cognitiva e sulla resilienza ai disturbi neurologici e psichiatrici.(31)
- Implicazioni: Il test per le varianti del gene BDNF potrebbe aiutare a prevedere la capacità di neuroplasticità di un individuo in risposta allo stress e potrebbe avere implicazioni per il recupero da insulti neurologici o traumi.(32)
Immagine: Una pagina di esempio del sito Analisi del test DNA Resilience.
Neuropeptide Y (NPY)
L'NPY è uno dei peptidi più abbondanti nel cervello ed è coinvolto nella regolazione delle risposte allo stress, dell'ansia e dell'assunzione di cibo. È considerato un agente ansiolitico endogeno.
- Associazioni genetiche: I polimorfismi nel gene NPY possono portare a differenze nell'espressione e nella secrezione di NPY, influenzando potenzialmente la resilienza allo stress di un individuo. Livelli più elevati di NPY sono generalmente protettivi contro gli effetti dello stress.
- Implicazioni Il test genetico per le varianti NPY può potenzialmente indicare la resilienza allo stress di base di un individuo e potrebbe predire la sua risposta psicologica allo stress cronico e ai traumi.(33)
Il ruolo dell'epigenetica nella modulazione della resilienza allo stress
Il campo della epigenetica si addentra in uno strato di complessità che va oltre la sequenza statica del DNA. Le modifiche epigenetiche consistono in cambiamenti chimici della struttura del DNA, come la metilazione e le modifiche degli istoni, che possono influenzare l'espressione dei geni senza alterare il codice genetico sottostante. Questi cambiamenti sono dinamici e rispondono agli stimoli ambientali, compreso lo stress cronico. L'esposizione a uno stress prolungato può portare ad alterazioni epigenetiche che influenzano il funzionamento dei geni coinvolti nella risposta allo stress, rendendo potenzialmente più difficile per gli individui gestire efficacemente nuovi fattori di stress.(34-35)
Le aziende all'avanguardia nella medicina personalizzata si stanno ora avventurando nell'epigenetica, cercando di scoprire come queste modifiche possano contribuire alla capacità di un individuo di resistere e riprendersi dallo stress. Analizzando i marcatori epigenetici, gli scienziati possono ottenere informazioni sullo stato attuale dei profili di espressione genica, che derivano sia dalla predisposizione genetica sia dalle influenze ambientali. Questi test possono identificare i cambiamenti epigenetici in risposta allo stress cronico, fornendo un'istantanea dei meccanismi molecolari che contribuiscono alla risposta allo stress di un individuo o alla sua mancanza.
Inoltre, la comprensione di questi cambiamenti epigenetici apre le porte a interventi personalizzati. Per invertire le modificazioni epigenetiche avverse, si potrebbero raccomandare specifici cambiamenti nello stile di vita, aggiustamenti dietetici e strategie terapeutiche. Questo approccio personalizzato non solo migliora la resilienza di un individuo, ma contribuisce anche alla più ampia comprensione di come lo stress impatti i nostri sistemi biologici a livello epigenetico, il che potrebbe portare a nuovi trattamenti e strategie preventive per i disturbi legati allo stress. Mappando il paesaggio epigenetico della risposta allo stress, possiamo iniziare a dipingere un quadro più completo dei fattori che contribuiscono alla nostra capacità unica di affrontare le sfide della vita.
Vantaggi e limiti dei test sul DNA della resilienza
Questi test possono offrire agli individui una migliore comprensione della loro innata resilienza e della loro risposta allo stress. Queste conoscenze potrebbero fornire strategie personalizzate per gestire lo stress e migliorare la salute mentale. Tuttavia, è essenziale affrontare questi test con cautela:
- Tratto complesso: La resilienza non è determinata da un singolo gene, ma è un tratto complesso influenzato da molti geni e fattori ambientali.
- Influenza ambientale: La genetica non funziona in modo isolato. Le esperienze di vita, i sistemi di supporto e le scelte di vita sono importanti per la resilienza.
- Potere predittivo: Sebbene questi test possano fornire indicazioni, non sono predittori definitivi della capacità di un individuo di affrontare le sfide della vita.
Conclusione
I test del DNA relativi alla resilienza rappresentano una frontiera intrigante per capire come il nostro patrimonio genetico possa influenzare la capacità di gestire lo stress e di riprendersi dalle avversità. Sebbene possano fornire indicazioni preziose, devono essere considerati come un pezzo del gigantesco puzzle che costituisce la resilienza di un individuo. Per chiunque sia interessato a questi test, si raccomanda di consultare un operatore sanitario o un consulente genetico per interpretare i risultati nel contesto più ampio della propria salute e del proprio stile di vita.
- Richiedete qui il vostro test del DNA integrale!
- Prenotate una consulenza per interpretare i vostri test di laboratorio e genetici con il Dr. Sovijärvi qui.
Riferimenti scientifici:
- Bobrow, M., & Grimbaldeston, A. H. (2000). Genetica medica, progetto genoma umano e salute pubblica: Presentato all'Università di Liverpool il 9 dicembre 1996 e accettato per la pubblicazione il 17 febbraio 2000. Journal of Epidemiology & Community Health, 54(9), 645-649.
- Cicchetti, D. (2010). La resilienza in condizioni di stress estremo: una prospettiva multilivello. Psichiatria mondiale, 9(3), 145.
- Luecken, L. J., & Gallo, L. C. (Eds.). (2008). Manuale dei metodi di ricerca fisiologica in psicologia della salute. Sage.
- Southwick, S. M., Vythilingam, M. e Charney, D. S. (2005). La psicobiologia della depressione e la resilienza allo stress: implicazioni per la prevenzione e il trattamento. Annu. Rev. Clin. Psychol., 1, 255-291.
- Michaud, M., Balardy, L., Moulis, G., Gaudin, C., Peyrot, C., Vellas, B., ... & Nourhashemi, F. (2013). Citochine proinfiammatorie, invecchiamento e malattie legate all'età. Journal of the American Medical Directors Association, 14(12), 877-882.
- Aguilera, G., Nikodemova, M., Wynn, P. C., & Catt, K. J. (2004). Recettori dell'ormone di rilascio della corticotropina: due decenni dopo. Peptidi, 25(3), 319-329.
- Subbannayya, T., Balakrishnan, L., Sudarshan, G., Advani, J., Kumar, S., Mahmood, R., ... & Prasad, T. K. (2013). Una mappa integrata della via di segnalazione dell'ormone di rilascio della corticotropina. Journal of cell communication and signaling, 7, 295-300.
- Binder, E. B. (2009). Il ruolo di FKBP5, un co-chaperone del recettore dei glucocorticoidi, nella patogenesi e nella terapia dei disturbi affettivi e d'ansia. Psychoneuroendocrinology, 34, S186-S195.
- Ising, M., Depping, A. M., Siebertz, A., Lucae, S., Unschuld, P. G., Kloiber, S., ... & Holsboer, F. (2008). I polimorfismi nella regione del gene FKBP5 modulano il recupero dallo stress psicosociale nei controlli sani. European Journal of Neuroscience, 28(2), 389-398.
- Vitellius, G., Trabado, S., Bouligand, J., Delemer, B., & Lombès, M. (2018, giugno). Fisiopatologia della segnalazione dei glucocorticoidi. In Annales d'endocrinologie (Vol. 79, No. 3, pp. 98-106). Elsevier Masson.
- Van West, D., Van Den Eede, F., Del-Favero, J., Souery, D., Norrback, K. F., Van Duijn, C., ... & Claes, S. (2006). Analisi del gene del recettore dei glucocorticoidi basata su SNP in pazienti con depressione maggiore ricorrente. Neuropsicofarmacologia, 31(3), 620-627.
- Schneider, K. K., Frings, C., Meyer, J., & Schote, A. B. (2016). Il ruolo del gene del recettore dei glucocorticoidi (NR3C1) per l'elaborazione degli stimoli di avversione. Neuroscience Research, 107, 8-13.
- Azadmarzabadi, E., Haghighatfard, A., & Mohammadi, A. (2018). Una bassa resilienza allo stress è associata ad alterazioni dell'espressione dei geni candidati nella via di segnalazione dopaminergica. Psicogeriatria, 18(3), 190-201.
- Heinz, A., & Smolka, M. N. (2006). Gli effetti del genotipo della catecol O-metiltransferasi sull'attivazione cerebrale suscitata da stimoli affettivi e compiti cognitivi. Reviews in the Neurosciences, 17(3), 359-368.
- Mier, D., Kirsch, P. e Meyer-Lindenberg, A. (2010). Substrati neurali dell'azione pleiotropica della variazione genetica nella COMT: una meta-analisi. Psichiatria molecolare, 15(9), 918-927.
- Mustapic, M., Maihofer, A. X., Mahata, M., Chen, Y., Baker, D. G., O'Connor, D. T., & Nievergelt, C. M. (2014). L'enzima biosintetico della catecolamina dopamina β-idrossilasi (DBH): la prima ricerca a livello genomico posiziona varianti che determinano il tratto e che agiscono in modo additivo nel promotore prossimale. Genetica molecolare umana, 23(23), 6375-6384.
- Vincent, S. e Robertson, D. (2002). La visione più ampia: le anomalie delle catecolamine. Clinical Autonomic Research, 12, I44-I49.
- Hoenicka, J., Aragüés, M., Ponce, G., Rodríguez-Jiménez, R., Jiménez-Arriero, M. A., & Palomo, T. (2007). Dai geni dopaminergici ai disturbi psichiatrici. Ricerca sulla neurotossicità, 11, 61-71.
- Hill, S. Y., Hoffman, E. K., Zezza, N., Thalamuthu, A., Weeks, D. E., Matthews, A. G., & Mukhopadhyay, I. (2008). Mutazioni dopaminergiche: Associazione all'interno della famiglia e linkage in famiglie con dipendenza da alcol multipla. American Journal of Medical Genetics Part B: Neuropsychiatric Genetics, 147(4), 517-526.
- He, Y., Martin, N., Zhu, G., & Liu, Y. (2018). Geni candidati per la ricerca di novità: una meta-analisi degli studi di associazione di: DRD4: esone III e: COMT: Val158Met. Genetica psichiatrica, 28(6), 97-109.
- Avula, R., Rand, A., Black, J. L., & O'kane, D. J. (2011). Genotipizzazione simultanea di polimorfismi multipli nel gene umano del trasportatore della serotonina e individuazione di nuove varianti alleliche. Translational psychiatry, 1(8), e32-e32.
- Tivol, E. A., Shalish, C., Schuback, D. E., Hsu, Y. P., & Breakefield, X. O. (1996). Analisi mutazionale del gene MAOA umano. American journal of medical genetics, 67(1), 92-97.
- Waider, J., Araragi, N., Gutknecht, L., & Lesch, K. P. (2011). La triptofano idrossilasi-2 (TPH2) nei disturbi del controllo cognitivo e della regolazione delle emozioni: una prospettiva. Psiconeuroendocrinologia, 36(3), 393-405.
- Bauer, M. E., & Teixeira, A. L. (2021). Neuroinfiammazione nei disturbi dell'umore: ruolo delle cellule immunitarie regolatorie. Neuroimmunomodulazione, 28(3), 99-107.
- Anderson, G., Kubera, M., Duda, W., Lasoń, W., Berk, M., & Maes, M. (2013). Aumento della trans-segnalazione dell'IL-6 nella depressione: focus sulla via del catabolita del triptofano, sulla melatonina e sulla neuroprogressione. Pharmacological Reports, 65(6), 1647-1654.
- Perry, B. I., Upthegrove, R., Kappelmann, N., Jones, P. B., Burgess, S., & Khandaker, G. M. (2021). Associazioni di proteine/trait immunologici con schizofrenia, depressione maggiore e disturbo bipolare: uno studio bidirezionale a randomizzazione mendeliana a due campioni. Cervello, comportamento e immunità, 97, 176-185.
- Bradley, J. (2008). La malattia infiammatoria mediata dal TNF. The Journal of Pathology: A Journal of the Pathological Society of Great Britain and Ireland, 214(2), 149-160.
- Loth, E., Poline, J. B., Thyreau, B., Jia, T., Tao, C., Lourdusamy, A., ... & Consorzio IMAGEN. (2014). Il genotipo del recettore dell'ossitocina modula l'attività striatale ventrale ai segnali sociali e la risposta agli eventi di vita stressanti. Psichiatria biologica, 76(5), 367-376.
- Myers, A. J., Williams, L., Gatt, J. M., McAuley-Clark, E. Z., Dobson-Stone, C., Schofield, P. R., & Nemeroff, C. B. (2014). La variazione del gene del recettore dell'ossitocina è associata a un aumento del rischio di ansia, stress e depressione in individui con una storia di esposizione a stress nelle prime fasi della vita. Journal of psychiatric research, 59, 93-100.
- Cowansage, K. K., LeDoux, J. E., & Monfils, M. H. (2010). Il fattore neurotrofico derivato dal cervello: un guardiano dinamico della plasticità neurale. Current molecular pharmacology, 3(1), 12-29.
- Chen, Z. Y., Jing, D., Bath, K. G., Ieraci, A., Khan, T., Siao, C. J., ... & Lee, F. S. (2006). Il polimorfismo della variante genetica BDNF (Val66Met) altera il comportamento legato all'ansia. science, 314(5796), 140-143.
- Phillips, C. (2017). Fattore neurotrofico di derivazione cerebrale, depressione e attività fisica: creare la connessione neuroplastica. Plasticità neurale, 2017.
- Schmeltzer, S. N., Herman, J. P., & Sah, R. (2016). Neuropeptide Y (NPY) e disturbo da stress post-traumatico (PTSD): un aggiornamento traslazionale. Neurologia sperimentale, 284, 196-210.
- Lux, V. (2016, marzo). Programmazione epigenetica nello sviluppo psicobiologico: Evidenza della teoria della doppia attivazione e ruolo mediatore dello stress precoce. In Qatar Foundation Annual Research Conference Proceedings Volume 2016 Issue 1 (Vol. 2016, No. 1, p. HBOP3415). Hamad bin Khalifa University Press (HBKU Press).
- Chukwuma Sr, C. (2022). L'epigenetica e la sua essenza nella comprensione della crescita, dello sviluppo e delle malattie umane. J Med Res, 8(5), 165-172.