Opettele olennaiset lisäravinteet oppaallamme kolmesta parhaasta luonnollisesta senolyytistä, jotka voivat nuorentaa soluja ja parantaa terveyttä. Ikääntyessämme solujen vanheneminen - kun solut lakkaavat jakautumasta ja kerääntyvät elimistöömme - voi johtaa erilaisiin ikään liittyviin sairauksiin. Tietyt luonnolliset yhdisteet on kuitenkin tunnistettu tehokkaiksi senolyyttejä jotka pystyvät selektiivisesti poistamaan näitä ikääntyneitä soluja. Tässä artikkelissa perehdytään syvällisemmin näiden merkittävien aineiden taustalla olevaan tieteeseen ja siihen, miten niitä voidaan sisällyttää päivittäisiin rutiineihin ikää ehkäisevien terveyshyötyjen saavuttamiseksi.
Johdanto
Ikääntyminen on monimutkainen biologinen prosessi, jolle on ominaista fysiologisten toimintojen asteittainen heikkeneminen ja lisääntynyt alttius sairauksille. Vaikka ikääntymistä on pitkään pidetty väistämättömänä osana elämää, viimeaikaiset edistysaskeleet biogerontologia on paljastanut sen taustalla olevia solu- ja molekyylimekanismeja. Näistä mekanismeista solujen vanheneminen on noussut merkittäväksi tekijäksi ikääntymiseen liittyvissä patologioissa. Se on peruuttamaton kasvupysähdys, jonka erilaiset stressitekijät laukaisevat.(1)
Koska vanhenevien solujen määrä kasvaa ikääntymisen myötä, on oletettu, että vanheneminen vaikuttaa ikääntymiseen. Senesenssiä tarvitaan estämään vaurioituneiden solujen leviäminen ja lisääntyminen, mikä laukaisee immuunijärjestelmän vasteen. Tämä solujen tarkistuspiste edellyttää tehokasta solujen korvausjärjestelmää, johon kuuluu sekä vanhenevien solujen poistaminen että progenitorisolujen mobilisointi optimaalisen solumäärän palauttamiseksi.(2)
Ydin-DNA-vaurio on usein raportoitu yleisesti senesenssin taustalla olevana syynä, pääasiassa DNA:n kaksoissäikeiden katkosten (DSB) muodossa, jotka aktivoivat DNA-vauriovasteen (DDR) reitin. Pitkittynyt DDR-aktivoituminen aktivoi senesenssin. Yksi tai muutama DDR-signaalia antava telomeeri (kromosomin pää) riittää käynnistämään solujen replikatiivisen senesenssin. Onkogeenien aktivoituminen on myös voimakas senesenssin laukaisija.(3)
Senesenssisolut ilmentävät huomattavia muutoksia sekretomissaan, joka on erityisen rikastunut proinflammatorisissa sytokiineissa ja matriksin metalloproteinaaseissa. Tästä käytetäänkin nimitystä senesenssiin liittyvä sekretorinen fenotyyppi (SASP).. Senesenssisoluilla on selviä fenotyyppisiä muutoksia, kuten litistynyt morfologia, muuttunut geenien ilmentyminen ja proinflammatoristen molekyylien eritys. Vaikka senesenssi aluksi toimii kasvaimia ehkäisevänä mekanismina pysäyttämällä vaurioituneiden solujen lisääntymisen, senesenssisolujen kertyminen ajan mittaan aiheuttaa kudoksen toimintahäiriöitä ja edistää ikääntymiseen liittyviä sairauksia. (4)
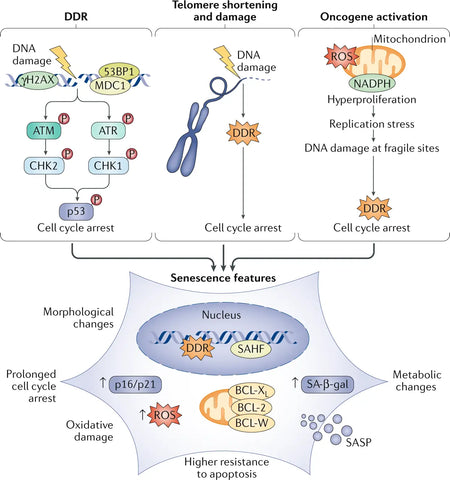
Kuva: Senesenssin ajurit ja fenotyypit.
Lähde: Di Micco, R., Krizhanovsky, V., Baker, D., & d'Adda di Fagagna, F. (2021). Solujen vanheneminen ikääntymisessä: mekanismeista terapeuttisiin mahdollisuuksiin. Nature Reviews Molecular Cell Biology 22 (2): 75–95.
Kun otetaan huomioon senesenssisolujen haitalliset vaikutukset kudosten homeostaasiin ja terveyteen, näihin soluihin kohdistaminen on noussut lupaavaksi terapeuttiseksi strategiaksi. Senolyytit ovat yhdisteitä, jotka on suunniteltu indusoimaan apoptoosia vanhenevissa soluissa ja säästämään samalla terveitä soluja valikoivasti. Niillä on mahdollisuus lievittää tulehdusta, tehostaa kudosten uudistumista ja parantaa ja viivästyttää ikääntymiseen liittyvien patologioiden puhkeamista.(5)
Senolyyttiset yhdisteet
Lukuisat luonnolliset ja synteettiset yhdisteet on tunnistettu potentiaalisiksi solunsalpaajiksi. senolyyttejä, joista kversetiini (luonnollinen yhdiste) ja dasatinibi (synteettinen lääke) ovat tämän luokan varhaisia ehdokkaita. Kvertsetiinin ja dasatinibin lisäksi useita muita yhdisteitä, kuten fisetiini, navitoklax ja ABT-263, ovat osoittaneet lupaavia senolyyttisiä ominaisuuksia prekliinisissä malleissa. Tässä artikkelissa käsitellään kolmea nykyisin saatavilla olevaa potentiaalista ja lupaavaa luonnollista senolyyttiä.
Fisetin
Fisetiini on bioaktiivinen flavonoli (polyfenoli), jonka potentiaalia edistää terveyttä ja pitkäikäisyyttä on tutkittu huomattavasti, pääasiassa lieventämällä solujen vanhenemista. Sitä on pääasiassa mansikoissa, omenoissa, persimonissa, sipuleissa, viinirypäleissä ja pieninä määrinä kurkkuissa (ks. kuva). Fisetiinillä on useita biologisia vaikutuksia, jotka johtuvat sen ainutlaatuisesta molekyylirakenteesta (tasomainen rakenne ja useita hiilirenkaita).(6-7)
Fisetiinin ominaisuuksien alustava tutkiminen paljastaa sen voimakkaan antioksidanttikapasiteetin, joka johtuu sen kyvystä suojata reaktiivisia happilajeja (ROS). Näin ollen sillä on ratkaiseva rooli solujen puolustautumisessa hapetusstressiä vastaan.(8)

Kuva: Fisetiinin ravinnonlähteet.
Lähde: Khan, N. & Syed, D. & Ahmad, N. & Mukhtar, H. (2013). Fisetiini: ravinnon antioksidantti terveyden edistämiseksi. Antioksidants & Redox Signaling 19 (2): 151–162.
Fisetiinin senolyyttinen aktiivisuus on ensisijainen painopiste pitkäikäisyystutkimuksessa. Solujen senesenssi on tila, jossa solut lakkaavat lisääntymästä ja kasautuvat ajan mittaan - se on osallisena erilaisissa ikääntymiseen liittyvissä sairauksissa (ks. tarkemmin edellä). Fisetiinin on havaittu indusoivan apoptoosia valikoivasti näissä vanhenevissa soluissa. Tämän selektiivisen poistumisen oletetaan lieventävän senesenssiin liittyviä fenotyyppejä ja siten osaltaan viivästyttävän tai ehkäisevän ikääntymiseen liittyviä patologioita. Verrattuna toiseen mahdolliseen senolyyttiseen yhdisteeseen fisetiini on noin kaksi kertaa voimakkaampi kuin kversetiini (ks. myöhemmin artikkelissa).(9-10)
Flavonoidien (kuten fisetiinin) prooksidanttinen aktiivisuus on tärkeä näkökohta, kun seulotaan senolyyttisiä aineita. Senesenssisolut keräävät runsaasti kuparia ja rautaa. Kversetiinin tai fisetiinin selektiivinen mekanismi liittyy nimenomaan kuparin/raudan edistämiin hapettumisvaurioihin vanhenevissa soluissa, jolloin apoptoosille vastustuskykyiset solut kuolevat.(11)
Fisetiini vaikuttaa myös ratkaiseviin solujen signaalireitteihin, jotka ovat olennainen osa ikääntymisprosessia. Se moduloi sirtuiinien (erityisesti SIRT1), mTOR:n (esto) ja JAK-STAT/NF-κB:n toimintaa, jotka ovat ratkaisevia solujen eloonjäämisen, apoptoosin ja autofagian säätelyssä. Näitä reittejä moduloimalla fisetiini voi teoriassa parantaa solujen toimintaa, vähentää tulehdusta ja ylläpitää kudosten homeostaasia.(12-14)
Fisetiinillä on myös osoitettu olevan neuroprotektiivisia ominaisuuksia. Se lieventää hermosolujen vaurioita ja parantaa kognitiivisia toimintoja ensisijaisesti antioksidatiivisen vaikutuksensa ja hermosolujen signaalireittien moduloinnin kautta.(15-16)
Näistä lupaavista prekliinisistä havainnoista huolimatta on tärkeää tunnustaa, että suurin osa fisetiiniä koskevasta tutkimuksesta on rajoittunut in vitro- ja eläinmalleihin. Näiden tulosten siirtäminen kliinisiin ihmissovelluksiin edellyttää tiukkoja kliinisiä tutkimuksia, joilla varmistetaan fisetiinin teho, turvallisuus ja optimaalinen annostelu. Onneksi joitakin kliinisiä tutkimuksia on jo käynnissä, ja tuloksia pitäisi saada lähivuosina.(17-18)
Kversetiini
Kversetiini on tärkeä antioksidantti, joka luokitellaan flavonoliksi. Sitä esiintyy luonnostaan monissa vihanneksissa, hedelmissä, marjoissa, lehdissä ja jyvissä. Kversetiiniä on pääasiassa kapriksissa, retiiseissä, tillissä, korianterissa, kaalissa, punasipulissa, parsakaalissa ja marjoissa, kuten karpaloissa ja puolukoissa. Kversetiini on yksi merkittävimmistä ja yleisimmistä luonnossa esiintyvistä flavonoleista.

Tutkimukset osoittavat, että kversetiini toimii viruksia, mikrobeja ja tulehduksia ehkäisevänä aineena.(19) Lisäksi tutkimukset osoittivat kversetiinin antihistamiinivaikutukset, mikä tarkoittaa, että se voi auttaa allergioiden hoidossa.(20-21) Merkittävin kversetiinin vaikutus ihmiskehoon on sen kyky vähentää hiljaista tulehdusta.(22)
Kvertsetiinin mahdollisuudet edistää pitkäikäisyyttä johtuvat sen antioksidanttisista ominaisuuksista. Antioksidanttina kversetiini tuhoaa vapaita radikaaleja ja vähentää hapetusstressiä elimistössä. Tutkimukset ovat osoittaneet, että kversetiini voi aktivoida sirtuiinit (erityisesti SIRT-1), jotka säätelevät soluprosesseja, kuten DNA:n korjausta, geeniekspressiota ja aineenvaihduntaa. Sirtuiinien aktivoituminen liittyy eliniän pidentymiseen eri organismeissa.(23-24)
Kversetiinin on myös osoitettu aktivoivan Nrf2-reittiä, ja soluytimissä se aktivoi erilaisten antioksidanttivaste-elementin (ARE) ohjaamien geenien transkriptiota. Nämä geenit säätelevät sytoprotektiivisten entsyymien, kuten glutationi-S-transferaasin, NAD(P)H-kvinonidehydrogenaasi 1:n ja hemioksygenaasi-1:n, ilmentymistä.(25)
Yleensä kversetiinilisät otetaan annoksena 500 mg kahdesti päivässä. Kversetiinin optimaalista annostusta ei kuitenkaan ole vielä määritetty. Kversetiinin suositeltu ravintosisältö on yleensä 5-40 mg päivässä, mutta sitä voidaan nauttia myös huomattavasti suurempia määriä (> 500 mg).
Kversetiinin osalta suosituksemme on Purovitaliksen liposomaalinen muoto.
Apigeniini
Apigeniini (4′,5,7,-trihydroksiflavoni) on luonnossa esiintyvä flavonoidiyhdiste, jota esiintyy useissa kasveissa, kuten persiljassa, sellerissä ja sitrushedelmissä. Sitä on erityisen runsaasti kamomillakasvin kukissa. Apigeniinillä on potentiaalia auttaa ehkäisemään kroonisia sairauksia, kuten diabetesta, Alzheimerin tautia, masennusta, unettomuutta ja syöpää, ja sen hyötyjä on havaittu vivo-tutkimuksissa (eläin- ja ihmistutkimuksissa).(26)

Yksi apigeniinin lupaavimmista näkökohdista on sen kyky edistää solujen joustavuutta. Apigeniinin on osoitettu aktivoivan Nrf2-reittiä, joka on ratkaisevan tärkeä elimistön puolustautumisessa hapetusstressiä ja tulehdusta vastaan. Säätämällä antioksidanttisten entsyymien, kuten superoksididismutaasin, katalaasin ja glutationiperoksidaasin, ilmentymistä apigeniini auttaa suojaamaan soluja reaktiivisten happilajien (ROS) aiheuttamilta vaurioilta.(27)
Antioksidanttisten ominaisuuksiensa lisäksi apigeniinillä on osoitettu tulehdusta ehkäiseviä vaikutuksia. Sen on todettu estävän pro-inflammatoristen sytokiinien, kuten TNF-α:n, IL-1β:n ja IL-6:n, tuotantoa moduloimalla NF-κB-signalointireittiä ((28) Apigeniinia on tutkittu myös sen mahdollisten syövänvastaisten ominaisuuksien vuoksi. Tutkimukset ovat osoittaneet, että apigeniini voi indusoida apoptoosia (ohjelmoitua solukuolemaa) erilaisissa syöpäsolulinjoissa, kuten rinta-, eturauhas- ja paksusuolen syöpäsoluissa. Apigeniini edistää myös autofagiaa, mikä auttaa poistamaan toimimattomia soluelementtejä.(29-30)
Apigeniinia on tutkittu myös sen vuoksi, että se pystyy muokkaamaan ikääntymiseen liittyviä reittejä. Yksi tällainen reitti on insuliini/IGF-1-signalointireitti (IIS), jonka tiedetään vaikuttavan eliniän säätelyyn eri lajeissa. Apigeniinin on osoitettu estävän IIS-reittiä, mikä saattaa jäljitellä kalorimäärän rajoittamisen vaikutuksia, joka on vakiintunut interventio pitkäikäisyyden edistämiseksi.(31-32) Lisäksi apigeniini estää metaboliseen oireyhtymään liittyvää NAD+-ase CD38:a, mikä lisää solunsisäisiä NAD+-tasoja ja vähentää proteiinien globaalia asetylaatiota.(33) Senesenssin osalta erityisesti aigeniittipigeniini auttaa estämään jäljellä olevia vanhenevia soluja tuottamasta SASP:tä (senesenssiin liittyvä erittyvä fenotyyppi; ks. edellä) ja näin tukemaan solujen ja kudosten terveyttä.(34)
Apigeniinin annostelun osalta ei ole olemassa yleisesti suositeltua annosta apigeniinilisälle. Eläinmalleissa on kuitenkin käytetty tutkimuksissa annoksia, jotka vaihtelevat 25:stä 100:aan mg painokiloa kohti.(35) Lisäravinteet ovat yleensä 50-500 mg päivässä. Tehokkainta ja turvallisinta annostusta ei kuitenkaan ole vielä lopullisesti vahvistettu. Apigeniinia pidetään yleisesti ottaen turvallisena, mutta suuret annokset voivat olla vuorovaikutuksessa tiettyjen lääkkeiden kanssa.
Johtopäätös
Luonnollisten senolyyttisten aineiden potentiaalin analyysin päätteeksi on selvää, että fisetiinin, kversetiinin ja apigeniinin kaltaisilla yhdisteillä on merkittäviä senolyyttisiä ominaisuuksia, jotka voivat vaikuttaa merkittävästi ikääntymisprosessiin. Nämä aineet kohdistuvat erityisesti vanheneviin soluihin ja eliminoivat ne, ja näin ne puuttuvat perustavanlaatuiseen ikääntymismekanismiin ja siihen liittyviin patologioihin. Näiden bioaktiivisten yhdisteiden sisällyttäminen ruokavalioon - jotka ovat peräisin esimerkiksi mansikoista, sipulista ja kamomillasta - on strateginen lähestymistapa solujen toiminnan parantamiseen ja soluvaurioiden kasautumisen lieventämiseen ajan myötä.
Vaikka prekliiniset tiedot ovat lupaavia, näiden havaintojen siirtäminen käytännön kliinisiin strategioihin edellyttää kuitenkin empiiristä lisätutkimusta tehokkuuden ja turvallisuuden validoimiseksi. Näin ollen näiden yhdisteiden jatkuva tutkiminen tiukoissa kliinisissä tutkimuksissa on edelleen ratkaisevan tärkeää.
Tieteelliset viitteet:
- Sikora, E., Arendt, T., Bennett, M., & Narita, M. (2011). Cellular senescence signature impact on ageing research. Ikääntymistutkimuksen katsaukset, 10(1), 146-152.
- He, S., & Sharpless, N. E. (2017). Senesenssi terveydessä ja sairaudessa. Cell, 169(6), 1000-1011.
- Di Micco, R., Krizhanovsky, V., Baker, D., & d'Adda di Fagagna, F. (2021). Solujen vanheneminen ikääntymisessä: mekanismeista terapeuttisiin mahdollisuuksiin. Nature Reviews Molecular Cell Biology 22 (2): 75–95.
- Kuilman, T. & Michaloglou, C. & Mooi, W. & Peeper, D. (2010). Senesenssin olemus. Genes & Development 24 (22): 2463–2479.
- Kirkland, J. L., & Tchkonia, T. (2020). Senolyyttiset lääkkeet: löydöstä translaatioon. Sisätautien aikakauskirja, 288(5), 518-536.
- Sengupta, B. & Banerjee, A. & Sengupta, P. (2005). Kasviflavonoidi fisetiinin vuorovaikutukset makromolekulaaristen kohteiden kanssa: näkemyksiä fluoresenssispektroskopisista tutkimuksista. Journal of Photochemistry and Photobiology B: Biology. 80 (2): 79–86.
- Bag, S. & Ghosal, S. & Karmakar, S. & Pramanik, G. & Bhowmik, S. (2023). Uncovering the Contrasting Binding Behavior of Plant Flavonoids Fisetin and Morin Having Subsidiary Hydroxyl Groups (- OH) with HRAS1 and HRAS2 i-Motif DNA Structures: Rakenteellisten muutosten ja sijaintivaikutusten purkaminen. ACS Omega 8 (33): 30315–30329.
- Khan, N. & Syed, D. & Ahmad, N. & Mukhtar, H. (2013). Fisetiini: ravinnon antioksidantti terveyden edistämiseksi. Antioksidants & Redox Signaling 19 (2): 151–162.
- Yousefzadeh, M. et al. (2018). Fisetiini on senoterapeutti, joka pidentää terveyttä ja elinikää. EBioMedicine 36: 18-28.
- Wyld, L. et al. (2020). Senesenssi ja syöpä: katsaus senesenssin ja senoterapioiden kliinisiin vaikutuksiin. Cancers 12 (8): 2134.
- Wang, Y. & He, Y. & Rayman, M. & Zhang, J. (2021). Flavonoideista peräisin olevien uusien senolyyttisten aineiden valikoiva mekanismi. Journal of Agricultural and Food Chemistry 69 (42): 12418–12423.
- Wiciński, M. et al. (2023). Natural Phytochemicals as SIRT Activators-Focus on Potential Biochemical Mechanisms. Nutrients 15 (16): 3578.
- Afroze, N. et al. (2022). Fisetiini estää solujen lisääntymistä, indusoi apoptoosia, lievittää oksidatiivista stressiä ja tulehdusta ihmisen syöpäsoluissa, HeLa. International Journal of Molecular Sciences 23 (3): 1707.
- Roy, T. et al. (2023). Fisetiinin kaksoiskohdennus mTOR/IL-17A:han ja autofagiaan lievittää psoriaasin kaltaista ihotulehdusta. Frontiers in Immunology 13: 1075804.
- Samanta, S. et al. (2022). Fisetiinin, luonnollisen flavonoidin, neuroprotektiiviset vaikutukset neurodegeneratiivisissa sairauksissa: Keskittyminen oksidatiivisen stressin rooliin. Frontiers in Pharmacology 13: 1015835.
- Singh, S. & Singh, A. & Garg, G. & Rizvi, S. I. (2018). Fisetiini kalorisen rajoituksen mimeettinä suojaa rotan aivoja ikääntymisen aiheuttamalta oksidatiiviselta stressiltä, apoptoosilta ja neurodegeneraatiolta. Life Sciences 193: 171–179.
- Verdoorn, B. et al. (2021). Fisetiini COVID-19:lle ammattitaitoisissa hoitolaitoksissa: Senolyyttiset kokeet COVID-aikakaudella. Journal of the American Geriatrics Society 69 (11): 3023–3033.
- Kirkland, J. (2024). Alleviation by Fisetin of Frailty, Inflammation, and Related Measures in Older Women (AFFIRM). ClinicalTrials.gov ID: NCT03430037.
- Chirumbolo, S. (2010). Kversetiinin, flavonolien ja flavonien rooli tulehdussolujen toiminnan moduloinnissa. Inflammation & Allergy-Drug Targets (Tulehdus ja allergia-lääkkeiden kohteet). 9 (4): 263–285.
- Chirumbolo, S. (2011). Kversetiini potentiaalisena allergialääkkeenä: mitä näkökulmia? Iran Journal of Allergy Asthma and Immunology. 10 (2): 139–140.
- Sagit, M. et al. (2017). Kversetiinin tehokkuus allergisen nuhan kokeellisessa rotan mallissa. European Archives of Oto-Rhino-Laryngology -lehden arkisto 274 (8): 3087–3095.
- Li, Y. et al. (2016). Kversetiini, tulehdus ja immuniteetti. Nutrients 8 (3): 167.
- Costa, L. & Garrick, J. & Roquè, P. & Pellacani, C. (2016). Kversetiinin aiheuttaman hermosuojan mekanismit: Counteracting Oxidative Stress and More. Oxidative Medicine and Cellular Longevity. 2016: 2986796.
- Cui, Z. et al. (2022). Kversetiinin terapeuttinen käyttö ikääntymiseen liittyvissä sairauksissa: SIRT1 potentiaalisena mekanismina. Frontiers in Immunology 13: 943321.
- Suraweera, T. & Rupasinghe, H. & Dellaire, G. & Xu, Z. (2020). Nrf2/ARE-polun säätely ruokavalion flavonoidien avulla: Friend or Foe for Cancer Management? Antioksidants 9: 973.
- Salehi, B. et al. (2019). Apigeniinin terapeuttinen potentiaali. International Journal of Molecular Sciences 20 (6): 1305.
- Paredes-Gonzalez, X. et al. (2015). NRF2-välitteisen geeniekspression indusointi ravinnon fytokemikaalisilla flavoneilla apigeniinillä ja luteoliinilla. Biopharmaceutics & Drug Disposition 36 (7): 440–451.
- Ginwala, R. & Bhavsar, R. & Chigbu, D. & Jain, P. & Khan, Z. (2019). Flavonoidien potentiaalinen rooli kroonisten tulehdussairauksien hoidossa keskittyen erityisesti apigeniinin anti-inflammatoriseen aktiivisuuteen. Antioksidants 8 (2): 35.
- Shukla, S. & Gupta, S. (2010). Apigeniini: lupaava molekyyli syövän ehkäisyyn. Pharmaceutical Research 27: 962–978.
- Sung, B. & Chung, H. & Kim, N. (2016). Apigeniinin rooli syövän ehkäisyssä apoptoosin ja autofagian induktion kautta. Journal of Cancer Prevention 21 (4): 216-226.
- Pan, H. & Finkel, T. (2017). Keskeiset elinikää säätelevät proteiinit ja reitit. Journal of Biological Chemistry 292 (16): 6452–6460.
- Shukla, S. & Gupta, S. (2009). Apigeniini tukahduttaa insuliinin kaltaisen kasvutekijä I:n reseptorin signalointia ihmisen eturauhassyövässä: In vitro- ja in vivo -tutkimus. Molecular Carcinogenesis 48 (3): 243–252.
- Escande, C. et al. (2013). Flavonoidi apigeniini on NAD+ ase CD38:n estäjä: vaikutukset solujen NAD+-aineenvaihduntaan, proteiinien asetylaatioon ja metabolisen oireyhtymän hoitoon. Diabetes 62 (4): 1084–1093.
- Lim, H. & Park, H. & Kim, H. (2015). Flavonoidien vaikutukset bleomysiinin aiheuttamasta vanhenemisesta johtuvaan eritysfenotyypin muodostumiseen BJ-fibroblasteissa. Biokemiallinen farmakologia 96 (4): 337–348.
- Salehi, B. et al. (2019). Apigeniinin terapeuttinen potentiaali. International Journal of Molecular Sciences 20 (6): 1305.