The principal mecanismo fisiológico que afecta la estabilidad y el estado general de alerta durante el día laboral es la regulación del azúcar en la sangre. Mantener un nivel estable de azúcar en la sangre al evitar comer en exceso, picar continuamente y tener comidas frecuentes es clave para la productividad y la claridad mental.
Los picos y caídas constantes en el azúcar en la sangre son factores significativos en los cambios de humor. La hipoglucemia (bajo nivel de azúcar en la sangre) en particular puede causar ansiedad, irritabilidad y nerviosismo, generalmente precedido por una caída significativa en el rendimiento cognitivo. Por el contrario, para los diabéticos, un alto nivel de azúcar en la sangre se asocia con un rendimiento cognitivo deteriorado y estados de ánimo negativos. El azúcar en la sangre puede alcanzar un nivel bajo incluso en individuos sanos, por ejemplo, debido a ejercicio prolongado o ayuno.
La activación de las señales de hambre no necesariamente es precedida por un nivel de azúcar en la sangre hipoglucémico (fisiológicamente bajo) – generalmente, la sensación de hambre y el impulso de comer son desencadenados por una rápida disminución del azúcar en la sangre. Así, mantener un nivel constante de azúcar en la sangre reduce los antojos de hambre y ayuda a lograr un estado estable de alerta a lo largo del día laboral.
HORMONAS INVOLUCRADAS EN LA REGULACIÓN DEL AZÚCAR EN LA SANGRE
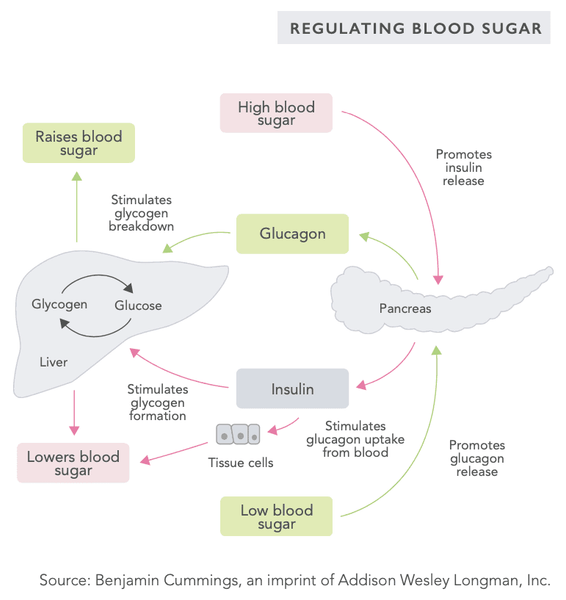
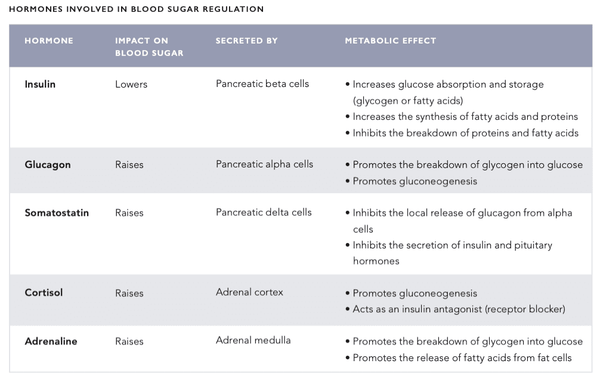
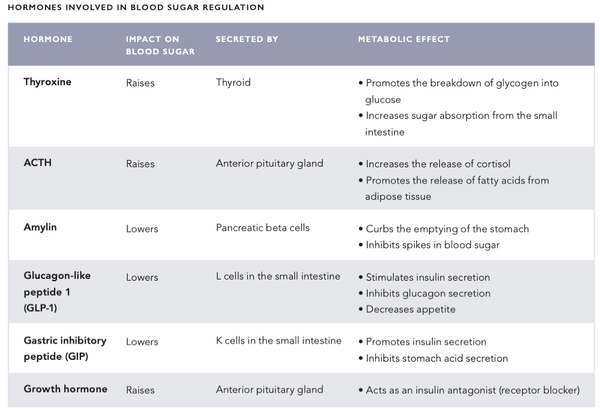
El mecanismo de regulación del azúcar en la sangre del cuerpo es un sistema muy sofisticado que involucra varias hormonas secretadas por órganos internos (ver la tabla en las páginas siguientes). El nivel de azúcar en la sangre se regula mediante un sistema de retroalimentación negativa – este sistema busca llevar al cuerpo a un estado de homeostasis sistémica, es decir, un estado de equilibrio.
Cuando el nivel de azúcar en la sangre es alto, pulsaciones de hormonas como la insulina se secretan en la circulación, reduciendo el nivel de azúcar en la sangre. Por el contrario, cuando el nivel de azúcar en la sangre es bajo, se secretan glucagón y otras hormonas en la circulación para elevar el nivel de azúcar en la sangre.
El monitoreo del nivel de azúcar en la sangre sistémico se lleva a cabo en las células beta de los islotes de Langerhans en el páncreas, así como en las neuronas sensoriales de glucosa del hipotálamo en el cerebro.
GLICOLISIS
La glicólisis es una parte simple del metabolismo de la glucosa en la que la glucosa se descompone en piruvato o lactato. Además de la producción de energía, la glicólisis regula la secreción de insulina y está vinculada a la secreción de insulina estimulada por glucosa en las células beta del páncreas. En tales casos, hay una secreción significativamente aumentada de la enzima glucocinasa que descompone la glucosa en glucosa-6-fosfato. Debido a que la actividad de la glucocinasa está fuertemente vinculada a los niveles de glucosa en sangre y, por lo tanto, a la secreción de insulina, la glucocinasa se considera el principal sensor del nivel de azúcar en la sangre.
GLUCONEOGÉNESIS
La gluconeogénesis es un proceso metabólico en el que se produce glucosa a partir de ácido láctico, glicerol, alanina y glutamina. La gluconeogénesis se activa particularmente cuando la dieta carece de carbohidratos. También permite al cuerpo estabilizar el nivel de azúcar en la sangre en caso de que se vuelva excesivamente bajo.
La gluconeogénesis tiene lugar principalmente en el hígado (alanina) y las cápsulas renales (glutamina) y, según los últimos estudios, también en los intestinos (particularmente en el intestino delgado).
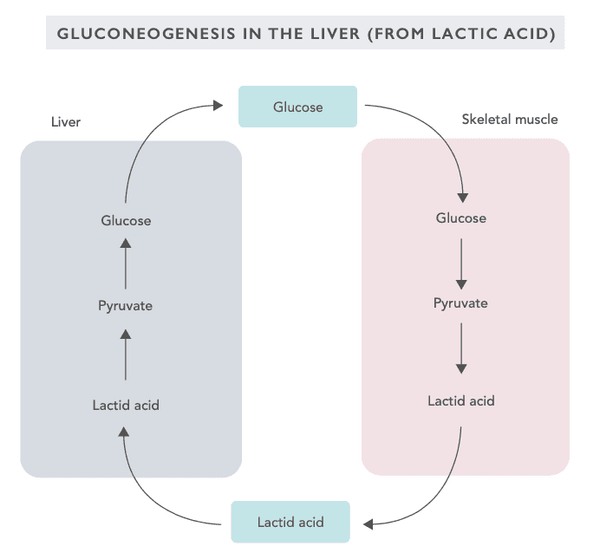
La gluconeogénesis se activa cuando una persona está en modo de inanición, siguiendo una dieta baja en carbohidratos, realizando ejercicio intenso o ayunando. La mayoría de las reacciones bioquímicas de la gluconeogénesis son inversas en comparación con las de la glicólisis. Las reacciones enzimáticas de la gluconeogénesis están reguladas por la hormona glucagón secretada por el páncreas.
GLICÓGENO
El glucógeno es una molécula de gran tamaño formada por varias (hasta 30,000) moléculas de glucosa. El glucógeno se almacena en el hígado (10 % del peso), en las células musculares (2 % del peso) y, en menor medida, en los glóbulos rojos. Además de la glucosa, el glucógeno se une a tres veces la cantidad de agua. Debido a esto, el peso corporal de una persona puede fluctuar varios kilogramos en un período de 24 horas dependiendo del nivel de llenado de las reservas de glucógeno.
El almacenamiento de glucógeno en el hígado actúa como una reserva de energía para las necesidades de producción de energía de todo el cuerpo, y en particular para las del sistema nervioso central. El almacenamiento de glucógeno en los músculos solo se utiliza para la producción de energía de las células musculares. La cantidad de glucógeno presente está determinada por el ejercicio físico, la tasa metabólica basal y los hábitos alimenticios.
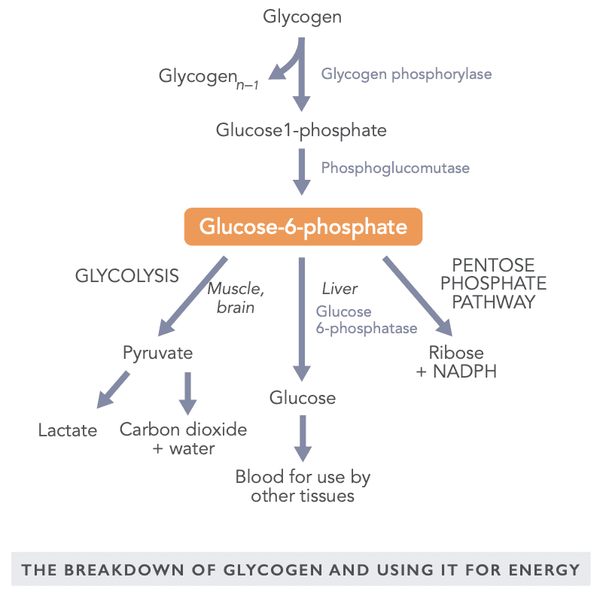
Las reservas de glucógeno son especialmente importantes para la regulación del azúcar en la sangre entre comidas y durante el ejercicio intenso. La glucosa también puede ser utilizada para energía en condiciones anaeróbicas. Por el contrario, los ácidos grasos se descomponen en energía solo en condiciones aeróbicas. El cerebro necesita un nivel constante de glucosa aunque puede utilizar, por ejemplo, los cuerpos cetónicos producidos por el hígado durante el ayuno.
Un producto de descomposición del glucógeno metabólicamente activo es el glucosa 6-fosfato en el que la molécula de glucosa se une a un grupo fosfato. Puede ser utilizado para energía en un músculo tanto en condiciones aeróbicas como anaeróbicas, utilizado a través del hígado como glucosa en otras partes del cuerpo o convertido en ribosa y NADPH para su uso en varios tejidos (por ejemplo, en la glándula adrenal, glóbulos rojos, glándulas mamarias y las células grasas en el hígado).
ALIMENTOS Y SUPLEMENTOS QUE AYUDAN A REGULAR LOS NIVELES DE AZÚCAR EN LA SANGRE
Los efectos de varios alimentos sobre el azúcar en la sangre se han descrito convencionalmente utilizando el índice glucémico (IG). Representa el cambio en el azúcar en la sangre causado por el alimento en comparación con un valor de referencia (solución de glucosa). Por el contrario, la carga glucémica (LG) indica el efecto total que la comida tiene sobre el azúcar en la sangre. Los conceptos de IG y LG fueron desarrollados originalmente para diabéticos. También ha habido intentos de aplicarlos al tratamiento de otros problemas de salud (como el cáncer y las enfermedades cardíacas) con resultados contradictorios. El IG y la LG han sido criticados por no considerar la variación individual y la respuesta de insulina desencadenada por los alimentos. Además, la respuesta glucémica desencadenada por una comida que consiste en varios ingredientes no puede ser estimada de manera confiable.
Sin embargo, se ha desarrollado un índice de insulina para representar mejor el efecto de los alimentos sobre la secreción de insulina. Hasta ahora, el índice de insulina ha recibido poca atención aunque parece ser útil para los diabéticos tipo 1 que anteriormente estaban acostumbrados a estimar y contar la cantidad de carbohidratos en la dieta. El índice de saciedad puede ser utilizado junto con el índice de insulina. Representa la sensación de saciedad que produce un alimento específico. Por ejemplo, las papas tienen un alto índice de insulina de 121, sin embargo, su puntaje de saciedad también es muy alto en 323 (ver la tabla en las páginas siguientes para más información).
Una dieta baja en IG es a menudo recomendada para individuos enfocados en la pérdida de peso. Sin embargo, el índice glucémico por sí solo parece tener poco impacto en la pérdida de peso en comparación con otras dietas de igual contenido calórico.
Según estudios, una dieta con una carga glucémica consistentemente alta está asociada con un nivel más alto de inflamación silenciosa. Por el contrario, la dieta mediterránea con una carga glucémica baja es bastante efectiva en la reducción de la obesidad, la resistencia a la insulina, la hipertensión y el colesterol alto, al menos en mujeres que sufren de síndrome metabólico según un estudio.
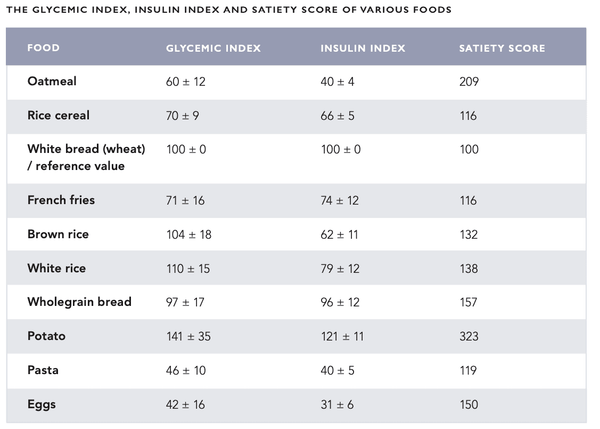
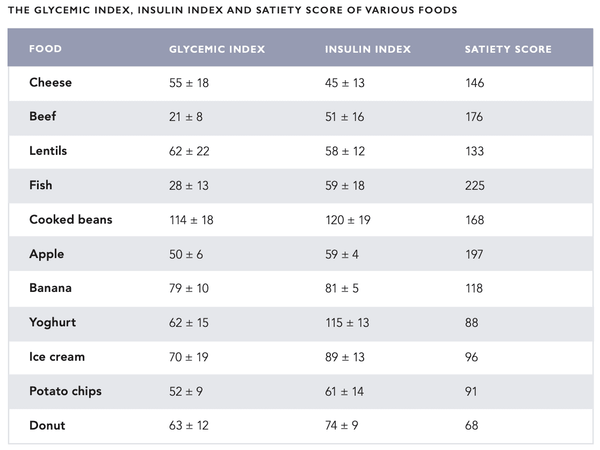
Una dieta de alimentos con una carga glucémica y un índice de insulina bastante bajos representa la opción preferida tanto para la salud como para la alerta mental. Los alimentos con un alto índice de insulina deben consumirse después del ejercicio para reponer las reservas de glucógeno en los músculos y el hígado con insulina.
El pico de azúcar en la sangre causado por una comida puede ser equilibrado con varios alimentos y suplementos (ver los capítulos siguientes). En los países occidentales, la canela se añade típicamente a los postres dulces y productos horneados que elevan significativamente los niveles de azúcar en la sangre. En China, los hongos y hierbas medicinales se incluyen en la dieta debido a sus propiedades equilibrantes del azúcar en la sangre.
se incluyen en la dieta debido a sus propiedades para equilibrar el azúcar en la sangre. La medicina ayurvédica de la India incorpora varias hierbas para equilibrar el azúcar en la sangre, como Gymnema Sylvestre. La palabra hindi ”gurmar” significa “destructor de azúcar”.
REGULANDO EL AZÚCAR EN LA SANGRE CON ALIMENTOS
La canela es una especia derivada de plantas del género Cinnamomum. La canela vendida en Europa es generalmente canela china (cassia) (Cinnamomum cassia, Cinnamomum aromaticum) que contiene cumarina, la cual es tóxica para el hígado y los riñones cuando se consume en grandes cantidades (ver el capítulo de Nutrición del Manual del Biohacker para más información).
Existen numerosas variedades de canela en el mundo con variaciones significativas en el contenido de cumarina. Consumir canela como té es una forma tradicional de usarla. Este método también reduce significativamente la ingesta de cumarina. La toxicidad de la cumarina varía entre individuos. Está vinculado a la capacidad de la variante genética CYP2A6 para actuar como parte del sistema de citocromo P450 del hígado.
Las propiedades de la canela que ayudan a regular el azúcar en la sangre y la sensibilidad a la insulina están fuertemente vinculadas a su alto contenido de cromo, así como a los efectos de los polifenoles y polímeros volátiles. Dependiendo del diseño del estudio y la dosis utilizada, la canela reduce los niveles de azúcar en la sangre en ayunas entre un 10 y un 29 %. Una cantidad diaria recomendada típica es de 1 a 6 gramos. Al decidir la cantidad a utilizar, se recomienda considerar su antecedentes genéticos (polimorfismo CYP2A6), objetivos y cualquier posible interacción con productos medicinales.
Los efectos de muchas hierbas que mejoran el rendimiento y de los llamados medicamentos inteligentes también están a menudo asociados con la regulación del azúcar en la sangre. Por ejemplo, según un metaanálisis de 2014, se ha encontrado que la raíz de ginseng ayuda a reducir los niveles de azúcar en la sangre en ayunas.
Alimentos y especias que ayudan a equilibrar el azúcar en la sangre:
- Canela
- Arándano
- Ajo
- Cereza ácida
- Vinagre de sidra de manzana
- Café
- Chía
- Comino
- Jengibre
- Hongo shiitake
- Limón
- Cúrcuma
- Cacao (y chocolate negro)
Suplementos y remedios que ayudan a equilibrar el azúcar en la sangre:
- Cromo
- Vitamina D
- Ácido alfa-lipoico
- Reishi
- Maitake
- Chaga
- Cordyceps
- Psyllium
- Aceite MCT
- Gymnema sylvestre
- Melón amargo
- Nopal
- Fenogreco
- Verdolaga
- Hoja de banaba
- Cardo mariano
- Resveratrol
- Magnesio
- Ginseng Panax
- Berberina
- Té verde
- Cilantro
- Sulfato de vanadio
COCTEL PARA BALANCEAR EL AZÚCAR EN LA SANGRE
Para ser consumido aproximadamente 30 minutos antes de una comida alta en carbohidratos:
- 100–300 mg de ácido alfa-lipoico
- 50–100 mg de cromo
- 500–1000 mg de berberina o 100-200 mg de dihidroberberina
- 200–400 mg de EGCG (extracto de té verde)
- 50 mg de resveratrol
- 100 mg de malato de magnesio
EL EFECTO DEL CAFÉ EN LA REGULACIÓN DEL AZÚCAR EN LA SANGRE
Los estudios a largo plazo han encontrado un vínculo entre el consumo de café y una mayor sensibilidad a la insulina, así como un menor riesgo de desarrollar diabetes tipo 2 (ver la sección “Café” en el capítulo de Nutrición del Manual del Biohacker para más información). A pesar de estos hallazgos, el café puede disminuir agudamente la sensibilidad a la insulina y aumentar los niveles de azúcar en la sangre en individuos no acostumbrados a la cafeína.
Los cambios en la regulación del azúcar en la sangre causados por el café se deben probablemente a la cafeína. No se ha encontrado que el café descafeinado cause un cambio similar en los niveles de azúcar en la sangre. Parece que el consumo regular de café también reduce los efectos del café sobre el azúcar en la sangre.
Los individuos con una mutación puntual en el gen CYP1A2 (variante 164A>C) descomponen la cafeína significativamente más lento en comparación con la población general. Esto también está relacionado con los cambios en el azúcar en la sangre causados por el café, así como con niveles más altos de azúcar en la sangre en ayunas, particularmente en individuos con hipertensión.
Para la mayoría de las personas, un consumo razonable de café (3–4 tazas al día) es compatible con una dieta saludable y equilibrada y un estilo de vida activo. Según un metaanálisis integral, un consumo razonable de café puede extender la esperanza de vida, reducir el riesgo de desarrollar diabetes tipo 2 y enfermedades cardiovasculares y prevenir la muerte prematura por estas enfermedades. Los beneficios para la salud del café se deben probablemente a los antioxidantes que contiene, como los polifenoles. De hecho, se han encontrado más de 1,000 compuestos antioxidantes en el café, incluso más que en el té verde y el cacao.

SUEÑO Y REGULACIÓN DEL AZÚCAR EN LA SANGRE
Los niveles de azúcar en la sangre caen constantemente cuando se ayuna durante las horas de vigilia. Por el contrario, los niveles de azúcar en la sangre generalmente permanecen constantes durante el sueño. Esto se debe a que el el nivel de azúcar en la sangre inicialmente aumenta aproximadamente un 20 % al comienzo del ciclo de sueño y luego cae lentamente a un nivel normal. Estas observaciones indican que la utilización de glucosa para energía disminuye durante el sueño. Durante el sueño no REM, el metabolismo de la glucosa del cerebro disminuye un 11 %. Por el contrario, el metabolismo de la glucosa aumenta durante el sueño REM y cuando se está despierto.

La privación del sueño tiene un impacto significativo en la regulación del azúcar en la sangre. La privación severa de sueño (cuatro horas de sueño por noche) durante tan solo una semana afecta el uso de glucosa para energía y eleva el azúcar en la sangre en ayunas. También es un factor predisponente para los trastornos del metabolismo del azúcar (prediabetes). Según un estudio, los individuos que duermen menos de 6.5 horas por noche tienen hasta un 40 % menos de sensibilidad a la insulina en comparación con aquellos que obtienen una cantidad normal (7–8 horas) de sueño por noche. La sensibilidad a la insulina deteriorada es un factor predisponente para los cambios en el azúcar en la sangre, la obesidad y la diabetes tipo 2. Según un metaanálisis publicado en 2015, para la regulación del azúcar en la sangre y la prevención de la diabetes, la cantidad óptima de sueño diario es de 7 a 8 horas. Vale la pena señalar que el exceso de sueño también puede afectar la regulación del azúcar en la sangre.
La privación del sueño también interfiere con la sensación de hambre al afectar la secreción de leptina y grelina. Según un estudio realizado en hombres jóvenes, la falta de sueño (4 horas) durante solo dos noches consecutivas disminuyó el nivel de la hormona de saciedad leptina en un 18 % y aumentó el nivel de la hormona del hambre grelina en un 28 %. Los individuos que experimentan privación del sueño informaron un aumento significativo (24 %) en el apetito, particularmente por alimentos dulces, salados o ricos en almidón. Los estudios poblacionales más completos también han arrojado resultados comparables.
Lee un artículo completo sobre cómo optimizar el sueño profundo y mejorar la calidad del sueño aquí.
EQUILIBRA TUS NIVELES DE AZÚCAR EN LA SANGRE FÁCILMENTE CON EL AYUNO INTERMITENTE
El ayuno intermitente significa ayunar durante una parte significativa del día (por ejemplo, 16 horas) y consumir la ingesta diaria de alimentos durante la ventana de alimentación restante (por ejemplo, 8 horas). La forma más sencilla de implementar esto es extender el ayuno nocturno omitiendo el desayuno y disfrutando de la primera comida del día por la tarde.
El concepto de ayuno intermitente contrarresta la tendencia de “seis comidas pequeñas al día” promovida por la industria alimentaria y la cultura del fitness de hoy. El pastoreo a menudo se racionaliza con afirmaciones de activar el metabolismo y facilitar el control del peso. Sin embargo, no hay base científica que respalde tales afirmaciones. De hecho, la tasa metabólica basal (TMB) aumenta ligeramente después de un ayuno de 36 horas – es solo después de 72 horas que la TMB comienza a disminuir lentamente.
El ayuno intermitente es útil para lograr la restricción calórica deseada cuando el objetivo es eliminar productos de desecho del cuerpo (autofagia) o pérdida de peso. Se han informado mejoras en la regulación del metabolismo del azúcar en conjunto con el ayuno intermitente.
Según un estudio, no hubo diferencias significativas en el gasto energético de los individuos que comían con frecuencia (6 veces al día) en comparación con aquellos que comían con menos frecuencia (2 veces al día). El mismo estudio encontró que aquellos que ayunaban por la mañana naturalmente comían ligeramente menos en general y también consumían una cantidad ligeramente menor de carbohidratos.
Desde una perspectiva evolutiva, los seres humanos evolucionaron para comer cuando hay comida disponible (generalmente por la tarde) – el resto del tiempo se dedicaba a adquirir la comida (por la mañana y durante el día).
En la práctica, el ayuno intermitente funciona bien ya que permite el consumo de comidas satisfactorias durante la ventana de alimentación mientras se mantiene una ingesta energética general moderada. Por ejemplo, el consumo de alimentos (particularmente carbohidratos) por la tarde reduce significativamente los niveles de hormonas del estrés y promueve el sueño así como estabilizando la secreción de leptina, grelina y adiponectina (quema de grasa). Consumir comidas más tarde por la tarde también activa el sistema nervioso parasimpático, calmando el cuerpo y facilitando el sueño.
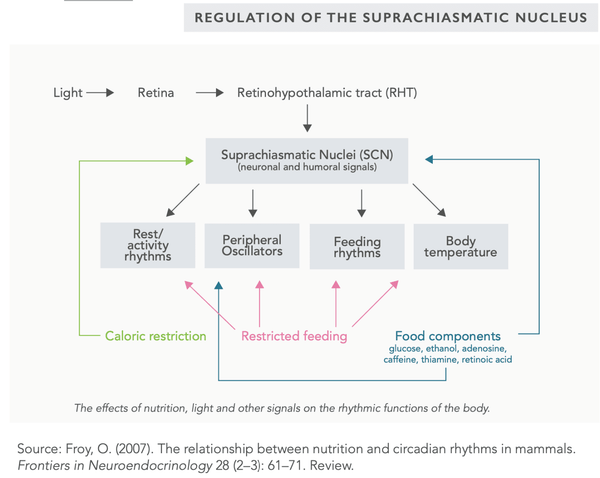
El ayuno intermitente (y la restricción calórica) también puede utilizarse para equilibrar la función del núcleo supraquiasmático (NSQ) que regula el ritmo circadiano del cuerpo. El factor principal en la regulación del NSQ es la luz (particularmente la luz solar).
El agua, el té, el café y el agua mineral se consumen a menudo para mantener el equilibrio de fluidos durante el ayuno. Los jugos verdes de baja energía también son una buena opción ya que contienen micronutrientes esenciales (ver recetas en la página siguiente). Las personas altamente activas o atléticas también pueden consumir aminoácidos esenciales (AAE) en forma de tabletas o polvo para maximizar la recuperación.
El ayuno intermitente (o el ayuno en general) no se recomienda generalmente para individuos menores de 18 años, embarazadas, lactantes, severamente fatigados o que padecen síndrome de fatiga crónica.
Existen varios métodos de ayuno intermitente:
- Ayuno durante 24 horas 1–2 veces por semana (”Eat Stop Eat”)
- Ayuno durante 20 horas seguido de una ventana de alimentación de 4 horas (”The Warrior Diet”)
- Ayuno durante 36 horas seguido de una ventana de alimentación de 12 horas (”The Alternate Day Fast”)
- Ayuno durante 16 horas seguido de una ventana de alimentación de 8 horas (”Leangains”)
- Ayuno durante 18 horas (café graso permitido) seguido de una ventana de alimentación de 6 horas (”Bulletproof Intermittent Fasting”)
Los beneficios para la salud del ayuno/ayuno intermitente incluyen:
- Puede extender la vida útil al ralentizar el proceso de envejecimiento
- Puede reducir el riesgo de desarrollar enfermedades metabólicas y crónicas como
- Cáncer
- Diabetes
- Síndrome metabólico
- Artritis
- Enfermedades neurodegenerativas (como la enfermedad de Alzheimer
- Puede mejorar la sensibilidad a la insulina y reducir la presión arterial
- Puede reducir el estrés oxidativo en el cuerpo
- Puede mejorar el equilibrio hormonal del cuerpo
LA GUÍA DEL BIOHACKER PARA EL AYUNO INTERMITENTE
Cada uno de los autores de el Manual del Biohacker tiene su propio patrón de ayuno intermitente que ha evolucionado a través de varios experimentos.
Aquí hay un patrón de muestra para una persona que es físicamente activa y trabaja en la oficina:
- Ayuno durante la noche y retrasar la primera comida tanto como sea posible (generalmente hasta algún momento entre las 3 PM y las 6 PM dependiendo del horario de la comida anterior)
- Mientras ayunas, bebe muchos líquidos como agua mineral (rica en minerales, retrasa el hambre)
- El hambre puede retrasarse aún más antes de la primera comida consumiendo una manzana que es rica en fibra y relativamente baja en energía (
- Considera las siguientes recetas de bebidas bajas en carbohidratos a continuación (imagen)
- La primera comida debe consistir principalmente en proteínas, verduras fibrosas y grasas, y una pequeña cantidad de carbohidratos (si se desea)
- La segunda (y última) comida, consumida entre las 8 PM y las 11 PM, debe incluir muchos carbohidratos así como cantidades adecuadas de grasas y proteínas – cuando se consume cerca de la hora de dormir puede ayudar a optimizar el sueño
- El ejercicio físico a menudo se programa al final del período de ayuno por la tarde o después de la primera comida más tarde en la noche.

Las elecciones de estilo de vida que mejoran la sensibilidad a la insulina incluyen:
- Dormir lo suficiente
-
Ejercicio regular (particularmente entrenamiento de fuerza y entrenamiento de alta intensidad)
- Combinar ejercicio aeróbico y entrenamiento de fuerza es la forma más efectiva de mejorar la sensibilidad a la insulina
- Manejo del estrés y reducción del estrés
- Pérdida de peso (particularmente alrededor de la cintura)
- Ingesta abundante de fibras solubles de los alimentos
- Comer más verduras coloridas, bayas y frutas (particularmente bayas oscuras como arándanos y grosellas negras)
-
Usar hierbas y especias en la cocina
-
Cúrcuma
-
Jengibre
-
Canela
- Ajo
- Ginseng
- Fenogreco
- Hongos medicinales (reishi, shiitake, maitake, chaga, cordyceps)
- Vinagre de sidra de manzana
- Té verde
-
Reducir la ingesta de carbohidratos, particularmente azúcares
-
Ayuno regular y ayuno intermitente
-
Evitar el sedentarismo excesivo
-
Eliminar aceites vegetales procesados y grasas trans de la dieta
-
Ciertos suplementos dietéticos pueden mejorar la sensibilidad a la insulina:
- Cromo
- Magnesio
- Berberina
- Resveratrol
- Ácido alfa-lipoico
MEDICIÓN Y MONITOREO DE LOS NIVELES DE AZÚCAR EN LA SANGRE
Un nivel constante de azúcar en la sangre es uno de los factores clave para el mantenimiento de buenos niveles de rendimiento y alerta mental. Para los diabéticos, monitorear los niveles de azúcar en la sangre es vital para la salud. Monitorear el propio nivel de azúcar en la sangre también puede ser útil para personas que no son diabéticas – como biohackers curiosos que desean descubrir qué factores en la nutrición y el estilo de vida tienen un efecto en el rendimiento y la alerta mental.
Las tiras de prueba de azúcar en la sangre se introdujeron en la década de 1970. Pronto fueron seguidas por dispositivos que proporcionaban un valor de azúcar en la sangre utilizando las tiras de prueba. Hoy en día, es posible tomar una muestra rápida del dedo y hacer que un dispositivo la analice casi instantáneamente. Dispositivos periféricos y aplicaciones diseñadas para medir el azúcar en la sangre también están disponibles para teléfonos inteligentes.
Los diabéticos ahora pueden usar monitores colocados bajo la piel que toman mediciones de azúcar en la sangre casi continuas (por ejemplo, cada cinco minutos). Estos monitores advierten al usuario cuando los resultados son demasiado bajos o demasiado altos o cuando se detectan cambios repentinos en el azúcar en la sangre. Es posible recopilar datos de azúcar en la sangre a largo plazo utilizando tales dispositivos.
El último avance es un dispositivo que utiliza láser (infrarrojo de longitud de onda media) para medir el azúcar en la sangre sin necesidad de una punción con aguja. Según un estudio realizado por los desarrolladores, la precisión del dispositivo es del 84 % en comparación con una prueba de sangre. También se están desarrollando varios dispositivos basados en nanotecnología.
Métodos de medición de azúcar en sangre en desarrollo:
- Lentes de contacto que miden los niveles de azúcar en sangre
- Dispositivos de infrarrojos y ultrasonido
- Espectroscopia Raman
- Nanobiosensores de un solo uso (análisis de azúcar en sangre a partir de saliva) y implantes (análisis de azúcar en sangre a partir de sangre)
- Sensores de afinidad que toman mediciones ópticamente
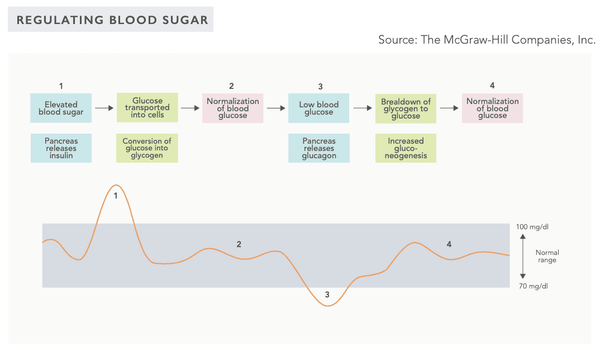
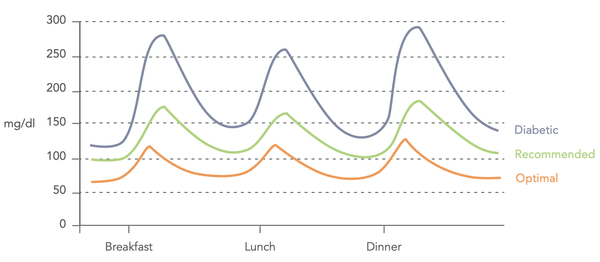 Imagen: Variaciones en los niveles de azúcar en la sangre (Manual del Biohacker, 2019).
Imagen: Variaciones en los niveles de azúcar en la sangre (Manual del Biohacker, 2019).
INTERPRETANDO MEDICIONES DE AZÚCAR EN LA SANGRE
Los siguientes valores recomendados se basan en varios estudios. Pueden usarse para determinar estimaciones óptimas del riesgo más bajo posible de desarrollar diabetes, enfermedades cardiovasculares, accidente cerebrovascular, síndrome metabólico, etc.
La ingesta de alimentos inmediatamente anterior debe tenerse en cuenta al medir los valores de azúcar en la sangre. Por ejemplo, los individuos que siguen una dieta baja en carbohidratos generalmente tienen una tolerancia reducida al azúcar, lo que puede causar valores de medición altos después de una comida alta en carbohidratos. Esto debe tenerse en cuenta al realizar una prueba de desafío de glucosa oral en un entorno de laboratorio. El período de ajuste recomendado es de cuatro días antes de la prueba, durante los cuales se debe consumir un mínimo de 150 g de carbohidratos por día.
-
Azúcar en sangre en ayunas (glucosa plasmática en ayunas, FPG)
- Normal: 4–6 mmol/L o 72–108 mg/dL
- Óptimo: 4.0–5.3 mmol/L o 72–95 mg/dL (La Fundación Life Extension recomienda 4.0–4.7 mmol/L o 72–85 mg/dL)
- Hemoglobina glicosilada (HbA1C)
- Normal: 20–42 mmol/L / 4.0 % – 6.0 %
- Óptimo: 20–34 mmol/L / 4.0 % – 5.3 %
- Los factores disruptivos pueden incluir anemia (resultado excesivamente bajo) o deshidratación (resultado excesivamente alto)
- Prueba de tolerancia a la glucosa oral (OGTT)
- Valores tomados: azúcar en sangre en ayunas y azúcar en sangre
- 1 hora y 2 horas después del desafío de glucosa (75 g)
- Valor normal a 1 hora:
- Valor normal a 2 horas:
- Medición de los niveles de azúcar en sangre a 1 hora y 2 horas después de una comida
- Automedición de los niveles de azúcar en sangre durante un período de 24 horas (tenga en cuenta que el margen de error al usar un monitor destinado a uso doméstico es aproximadamente del 10 %)
- Azúcar en sangre después de ayunar durante 12 horas
- Azúcar en sangre inmediatamente antes del almuerzo
- Azúcar en sangre una hora después del almuerzo (valor óptimo
- Azúcar en sangre 2 horas después del almuerzo (valor óptimo
- Azúcar en sangre 3 horas después del almuerzo (valor óptimo
Si deseas aprender a interpretar tus propios niveles de azúcar en la sangre y, sobre todo, qué puedes hacer para equilibrar tus niveles de azúcar en la sangre, te recomendamos tomar el curso en línea Optimiza tus Resultados de Laboratorio. A continuación se presenta material adicional del curso, por ejemplo, para medir la insulina y evaluar la sensibilidad a la insulina.
INSULINA EN AYUNO
La insulina es una hormona producida y secretada por las células beta en el páncreas. El cuerpo secreta insulina como respuesta a los niveles elevados de glucosa en sangre que son causados por la alimentación o la secreción de cortisol debido al aumento del estrés. La insulina aumenta la absorción y almacenamiento de glucosa y la síntesis de ácidos grasos y proteínas, mientras inhibe la descomposición de proteínas y ácidos grasos. Los niveles altos de insulina ocurren en conexión con la resistencia a la insulina, la obesidad, el síndrome metabólico, el insulinoma, el síndrome de Cushing o dosis excesivas de insulina o corticosteroides. Los niveles bajos de insulina ocurren en conexión con la diabetes, el hipopituitarismo y diversas enfermedades pancreáticas. Idealmente, el nivel de insulina en ayunas debería estar en el extremo inferior del rango de referencia.
La insulina inhibe la lipólisis, o la descomposición de grasa en energía. Si los niveles de insulina almacenados en el cuerpo están consistentemente elevados, los ácidos grasos que circulan en la sangre se almacenan en el tejido adiposo. Esto se llama lipogénesis. En particular, la secreción de insulina se estimula por niveles altos de azúcar en la sangre y una dieta rica en carbohidratos. La ingesta abundante de proteínas también aumenta la secreción de insulina. Debido a estos factores, el nivel de insulina en ayunas debería ser bastante bajo, en la mitad inferior del rango de referencia. Los niveles altos de insulina también pueden ser un factor predisponente para las enfermedades crónicas discutidas en la descripción del valor de HbA1C.
- Rango de referencia: 2.0–20 mIU/L
HOMA-IR (SENSIBILIDAD A LA INSULINA)
Al calcular la interacción entre la glucosa en ayunas y la insulina en ayunas, se puede evaluar la función de las células beta del páncreas y la sensibilidad a la insulina del cuerpo. La sensibilidad a la insulina depende de cuánto insulina necesita ser secretada para almacenar una cierta cantidad de glucosa. La sensibilidad a la insulina está presente cuando solo se necesita una pequeña cantidad de insulina para almacenar una cierta cantidad de glucosa en las células. Por el contrario, la resistencia a la insulina está presente cuando se requiere más insulina para almacenar una cantidad equivalente de glucosa.
La resistencia a la insulina y la baja sensibilidad a la insulina pueden llevar a diabetes tipo 2, enfermedad del hígado graso no alcohólico (NAFLD), enfermedad cardiovascular, acumulación de grasa visceral dañina o incluso cáncer. La sensibilidad a la insulina normal u óptima generalmente se asocia con una mejor salud y metabolismo.
///






