Alt, hvad du har brug for at vide om aldring og anti-aldringsprocesser. Hvordan vender man aldring? Hvad er de 9 kendetegn ved aldring? Læs mere for at finde ud af det!
I 2013 udgav Carlos López-Otín og hans kolleger en banebrydende artikel, hvor de forsøgte at identificere og kategorisere de cellulære og molekylære kendetegn ved aldring.. De foreslog ni kandidatkendetegn, som generelt anses for at bidrage til aldringsprocessen og tilsammen bestemme den aldrende fænotype. López-Otín et al. definerede, at et kendetegn ideelt set skulle opfylde de tre følgende kriterier: Det skulle manifestere sig under normal aldring, dets eksperimentelle forværring skulle fremskynde aldringen, og dets eksperimentelle forbedring skulle forsinke den normale aldringsproces og dermed øge den sunde levetid.
De oprindelige ni kendetegn ved aldring
Nøglen til at bremse eller endda vende aldring er ikke baseret på ideen om bare at øge levetiden, men sundhedsspændvidde (den periode af livet, der tilbringes ved godt helbred, fri for kroniske sygdomme og handicap som følge af aldring). Der har ikke været så meget kompression af sygelighed til dato, fordi vi har reduceret dødeligheden mere, end vi har forhindret sygelighed. Sundhedsspændvidden (at have sunde leveår) øges, når sygeligheden (at lide af en sygdom eller en medicinsk tilstand) mindskes, mest effektivt ved at hæve debutalderen.
Vellykket og sund aldring kan defineres på følgende måde:
- Lav sandsynlighed for sygdom eller handicap
- Høj kognitiv og fysisk funktionsevne
- Aktivt engagement i livet
De foreslåede ni kendetegn ved aldring er grupperet i tre kategorier:
- 1. Primære kendetegn (Årsager til skader)
- De udløsende faktorer, hvis skadelige konsekvenser gradvist akkumuleres med tiden. Alle utvetydigt negative.
- 2. Antagonistiske kendetegn (reaktioner på skade)
- Modsatte effekter af de primære kendetegn. Ved lave niveauer formidler de gavnlige effekter, men ved høje niveauer bliver de skadelige (f.eks. senescens).
- 3. Integrative kendetegn (De skyldige i fænotypen)
- Slutresultatet af de to foregående grupper af kendetegn og akkumulerede skader, som ikke kan kompenseres af vævshomøostatiske mekanismer. Disse er i sidste ende ansvarlige for den funktionelle nedgang, der er forbundet med aldring.
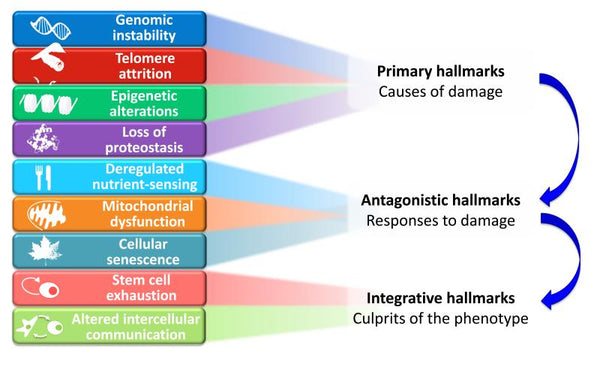
Billede: Funktionelle forbindelser mellem aldringens kendetegn.
Kilde: López-Otín, C. & Blasco, M. & Partridge, L. & Serrano, M. & Kroemer, G. (2013). Aldringens kendetegn. Celle 153 (6): 1194–1217.
1. Genomisk ustabilitet
DNA's integritet og stabilitet udfordres løbende af eksterne fysiske, kemiske og biologiske stoffer samt af interne trusler, der omfatter DNA-replikationsfejl, spontane hydrolytiske reaktioner og produktion af reaktive oxygenarter. Disse fører i sidste ende til til ophobning af genetiske skader gennem hele livet.
Måder at forbedre genomisk stabilitet på (kendetegn #1):
- Antioxiderende mikronæringsstoffer (selen, zink, C-vitamin, E-vitamin) ->. begrænser DNA-læsioner
- Afhjælper selv små mangler på folat, B12-vitamin, niacin og zink ->. har en betydelig indvirkning på frekvensen af spontane kromosomskader
- Ganoderma lucidum (reishi) glucaner
- Polyfenoler -> fjerner frie radikaler
- Moderat og "selvreguleret" motion
- Undgå følgende:
- Stråling og kemisk eksponering
- Eksponering for tungmetaller
- Nikkel, cadmium og arsenik, i særdeleshed
- Rygning af cigaretter
- Sidder for længe
- Overdreven brug af alkohol, energidrikke og mælk
2. Nedslidning af telomerer
Telomerer er særligt modtagelige for aldersrelateret forringelse. Telomerforkortelse observeres under normal aldring både hos mennesker og mus. Telomerer er bundet af et multiproteinkompleks kaldet shelterinsom forhindrer DNA-reparationsproteiner i at få adgang til telomererne (uden det ville telomererne blive "repareret" som DNA-brud, hvilket ville føre til kromosomfusioner). DNA-skader på telomerer er bemærkelsesværdigt konstante og meget effektive til at fremkalde aldring.
Måder at reducere forkortelse af telomerer (kendetegn #2):
- Øg indtaget af antioxidanter i kosten
- Højt indtag af omega-3-fedtsyrer, især
- Optimering af D-vitamin, B12-vitamin og folat niveauer i blodet
- Middelhavskost
- Undgå følgende:
- Rygning
- Fedme
- Eksponering for giftstoffer og forurening
- Balance i stressniveauer
- Balance mellem træningsrutine og intense træningspas
- Meditation med kærlig venlighed & Mindfulness-meditation praksis (og meditation i almindelighed)
- Hyperbarisk iltbehandling (HBOT)
- Gynostemma, gotu kola og astragalus-urter (muligvis effektiv)
- Hvad der ikke virker: Langvarig kaloriebegrænsning
3. Epigenetiske ændringer
Mange former for epigenetiske ændringer påvirker alle celler og væv gennem hele livet (forårsaget af ting som kost, kemikalier, medicin, sollys, varme/kulde, motion osv.) Epigenetiske ændringer forudsætter ændringer i DNA-methyleringsmønstre, posttranslationel modifikation af histoner og remodellering af kromatin.Medlemmer af sirtuin-familien af NAD-afhængige proteindeacetylaser og ADP-ribosyltransferaser er blevet grundigt undersøgt som potentielle anti-aldringsfaktorer - hos mennesker bidrager mindst tre medlemmer af sirtuin-familien, SIRT1, SIRT3 og SIRT6, til sund aldring.
Måder til at håndtere epigenetiske ændringer (Hallmark #3):
- Optimer methyleringsveje (folat, B12, B6, TMG)
- Aktivatorer af Sirtuin-veje (SIRT1, SIRT3, SIRT6):
- Spermidin (hæmmer histondeacetylaser)
- Periodisk kaloriebegrænsning og periodisk faste
- Regelmæssig (intens) motion
- Optimering af søvn (søvnunderskud forårsager skadelige epigenetiske ændringer)
- Metformin (bivirkninger er advarslen); helst (dihydro)berberin
- Alfa-ketoglutarat (CaAKG)
- Få regelmæssigt hormetiske doser af varme, kulde, sollys osv. ("giften ligger i dosen")
- Epigenetiske lægemidler under udvikling der er rettet mod DNA-methyltransferase, histondeacetylase, histonmethyltransferase og kromatin
Anbefalede kosttilskud:
Purovitalis Liposomal Quercetin
Purovitalis Liposomal Resveratrol
4. Tab af proteostase
Proteostase omfatter mekanismer til stabilisering af korrekt foldede proteiner (især heat-shock-familien af proteiner) og mekanismer til stabilisering af korrekt foldede proteiner. nedbrydning af proteiner ved hjælp af proteasomet eller lysosomet.. Flere undersøgelser har vist, at proteostase ændres med aldring hvilket fører til kronisk ekspression af ufoldede, fejlfoldede eller aggregerede proteiner. Disse bidrager til udviklingen af nogle aldersrelaterede degenerative sygdommesåsom Alzheimers sygdom.
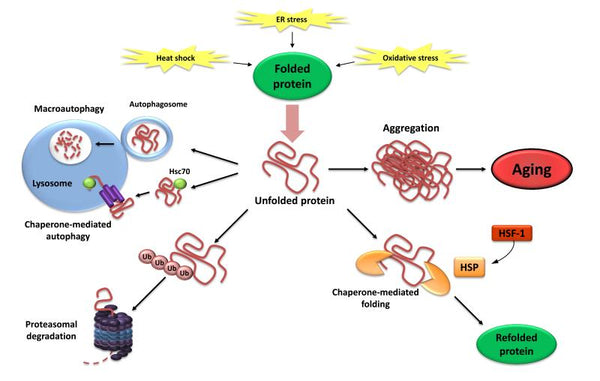
Billede: Tab af proteostase. Manglende refoldning eller nedbrydning af ufoldede proteiner kan føre til ophobning og aggregering af dem, hvilket resulterer i proteotoksiske effekter.
Kilde: López-Otín, C. & Blasco, M. & Partridge, L. & Serrano, M. & Kroemer, G. (2013). Aldringens kendetegn. Celle 153 (6): 1194–1217.
Måder at forbedre proteostasens stabilitet på (kendetegn 4):
Generelt er den bedste måde at beskytte kroppen mod tab af proteostase ved at aktivere autofagi.
- Faste, intermitterende kaloriebegrænsning (langvarig er ikke nyttig!), ketose, motion (bedst i fastende tilstand), styrketræning, kulde & udsættelse for varmedyb søvn (og melatonin)
- Sulforafan, kaffe, curcumin, polyfenoler, EVOO, resveratrol, grøn te, spermidin
- Senolytiske næringsstoffer og kosttilskud:
- Quercetin, fisetin, luteolin, curcumin, piperlongumine, molekylær brint (H2) osv.
- AMPK-aktivatorer:
- Berberin (DHB endnu bedre), resveratrol (og pterostilben), hesperidin, ginsenosider, quercetin, curcumin, naringenin, gynostemma, crocin (i safran), salvianolsyre B, alfa-liponsyre osv.
- Metformin og rapamycin (Nb. pos.sible bivirkninger)
- Hsp70 (heat-shock protein 70)-induktorer:
- Sauna og udsættelse for varme
- Shikonin (fra rødderne af shikonin-planten)
- Specifikke senolytiske lægemidler (såsom Dasatinib og Navitoclax)
5. Dereguleret næringsstof-fornemmelse
IGF-1- og insulinsignalering er kendt som IIS-vejen, som er den mest bevarede aldringskontrollerende vej i evolutionen. Ud over IIS-stien, der deltager i glukosesansning, er der der yderligere tre relaterede og indbyrdes forbundne næringsstofsensoriske systemermTOR (registrering af høje aminosyrekoncentrationer), AMPK (registrering af lavenergitilstande ved at registrere høje AMP-niveauer) og sirtuiner (registrering af lavenergitilstande ved at registrere høje NAD+-niveauer). For at opsummere er der stærke beviser for, at anabolsk signalering (mTOR, højt insulinindhold) fremskynder aldring, og at nedsat næringssignalering (AMPK, lavt insulinindhold) forlænger levetiden.
Måder at håndtere dereguleret næringsstofsensorik (kendetegn #5):
Praktisk talt alle de tidligere måder at håndtere kendetegn 1-4 på er dækket af sensibilisering og genregulering af næringsstofsensorik. Disse omfatter:
- kostrestriktioner
- Aktivering af AMPK
- sirtuin-aktivering
- Hormesis
- reduktion af oxidativ stress og inflammation
- øge autofagi
6. Mitokondriel dysfunktion
Mitokondrie-dysfunktion har vist sig at øge aldringsprocessen. Når en organisme ældes, mindskes effektiviteten af cellernes respirationskæde, hvilket fører til elektronlækage og reduceret ATP-generering.. Den reducerede effektivitet af mitokondriel bioenergetik med aldring kan skyldes flere krydsende mekanismerherunder reduceret biogenese af mitokondrier, ophobning af mutationer og deletioner i mtDNA, oxidativ stress i mitokondrieproteiner, destabilisering af respirationskæden, ændringer i mitokondriemembranernes lipidsammensætning og ændringer i mitokondriernes dynamik.
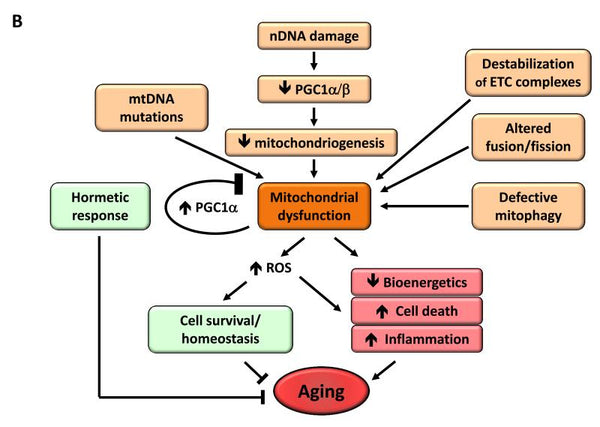
Billede: Mitokondriel dysfunktion og dens effekt på aldring.
Kilde: López-Otín, C. & Blasco, M. & Partridge, L. & Serrano, M. & Kroemer, G. (2013). Aldringens kendetegn. Celle 153 (6): 1194–1217.
Måder at håndtere mitokondriel dysfunktion på (kendetegn #6):
- Aktiver mitohormesis med:
- Intermitterende kaloriebegrænsning
- Intermitterende faste
- Træning
- Udsættelse for kulde
- Fytonæringsstoffer (såsom flavonoider)
- Målrettet Nrf2-stien (homeostase og strukturel integritet) med:
- Varme- og kuldeeksponering
- Fysisk træning
- Periodisk faste og ketose
- Sulforafan, polyfenoler, quercetin, curcumin osv.
- Molekylær brint (H2) -> Anbefaling af produkt
- Forbedre mitokondriebiogenese og -reparation (aktivering af PGC-1α):
- Fysisk træning
- Ketose og ketonstoffer
- Acetyl-L-carnitin
- Polyfenolerquercetin
- Rhodiola rosea (salidrosider)
- Coenzym Q10, pyrroloquinolinkinon (PQQ), nikotinamidmononukleotid (NMN), alfa-liponsyre (ALA)
7. Cellulær senescens
Fordi antallet af senescente celler stiger med alderen, er det blevet antaget, at senescens bidrager til aldring. Senescens er imidlertid nødvendig for at forhindre distribution og spredning af beskadigede celler, der udløser en reaktion fra immunsystemet. Dette cellulære kontrolpunkt kræver et effektivt celleudskiftningssystem, der involverer både fjernelse af senescente celler og mobilisering af progenitorceller for at genoprette det optimale antal celler. Senescente celler udtrykker betydelige ændringer i deres sekretom, som især er beriget med proinflammatoriske cytokiner og matrixmetalloproteinaser. Det kaldes derfor den "senescens-associerede sekretoriske fænotype".
Måder at bekæmpe cellulær senescens på (kendetegn #7):
Senescente celler holder til sidst op med at formere sig, men de dør ikke, når de skal, som almindelige celler gør. I stedet bliver de og fortsætter med at frigive kemikalier, der kan udløse inflammation og immunrespons.
Senolytiske forbindelser der selektivt retter sig mod senescente celler omfatter:
- Fisetin (også kaldet "det ultimative senolytiske middel")
- Quercetin
- Theaflaviner
- Apigenin
- Tocotrienoler (form af E-vitamin)
- Piperlongumine
- Molekylær brint (H2)
8. Udmattelse af stamceller
Voksne stamceller er i stand til at forny sig selv og differentiere sig til flere celletyper i et væv. Selvom fænotyper og mekanismer varierer meget, falder alle stamcellepopulationer i funktion med alderen. Udtømning af stamceller er den samlende konsekvens af forskellige aldringsrelaterede skader og udgør sandsynligvis en af de ultimative syndere i cellulær aldring.. Undersøgelser af ældre mus har afsløret et generelt fald i cellecyklusaktiviteten hos hæmatopoietiske stamceller (HSC'er)hvilket korrelerer med ophobningen af DNA-skader og overekspression af cellecyklusinhiberende proteiner (f.eks. p16INK4a). Telomerforkortelse har også vist sig at være en vigtig årsag til nedgangen i stamceller ved aldring.
Måder at modvirke udmattelse af stamceller (kendetegn #8):
- Stamcellebehandling (autolog vs. allogen & forskellige celletyper)
- Stamcelleterapi er stadig et "wild west". Der er potentielle bivirkninger og risicisom f.eks. vækst af tumorer og kræft.
- Fotobiomodulation ("terapi med rødt lys")
- PBM stimulerer forskellige typer stamceller til at øge deres migration, spredning og differentiering in vitro og in vivo.
- Gendanner ældre stamceller ved at angribe giftige metabolitter:
- Aktiverer sirtuiner - SIRT1 & SIRT 3 (se #3 & #4)
- N-acetyl cystein (NAC)
- Forbedrer proteostasens stabilitet (se #4)
- Forbedre mitokondriefunktionen (se #6)
- Brug senolytika (se #7)
- Gendan epigenetisk hukommelse (se #3)
- Optimer D-vitamin-niveauerne
- Spirulina (in vitro-undersøgelse)
9. Ændret intercellulær kommunikation
Cellulær aldring finder også sted på niveauet for intercellulær kommunikation. Disse omfatter neurohormonal signalering (øgede inflammatoriske reaktioner), immunovervågning (patogener og præmaligne celler) og ændringer i det ekstracellulære miljø. Aldring på grund af inflammation kaldes inflammaging. Det kan skyldes flere årsager, f.eks. ophobning af proinflammatorisk vævsskade, et dysfunktionelt immunsystems manglende evne til effektivt at fjerne patogener og dysfunktionelle værtsceller og forekomsten af en mangelfuld autofagisk reaktion. Aldringsændringer i ét væv kan føre til aldringsspecifik forringelse af nabovævet: Senescente celler inducerer senescens i deres tilstødende celler via gap-junction-medierede celle-celle-kontakter og processer, der involverer reaktive oxygenarter. Dette fænomen kaldes også en sensecent cell bystander-effekt.
Måder at forbedre intercellulær kommunikation (kendetegn #9):
- Lavere generel inflammation i kroppen
- En overordnet anti-inflammatorisk livsstilstilgang
- Brug molekylær brint (H2)
- Flere anti-aldringseffekter i kroppen (herunder reduktion af inflammation)
- Lavere oxidativ stress i kroppen og reduktion af reaktive iltarter (ROS)
- Øge autofagi i kroppen (se før)
- Behandle tarmdysbiose og forbedre diversiteten og den generelle sundhed i tarmens mikrobiota
- Behandle muligt utæt tarmsyndrom
10. Stivhed i den ekstracellulære matrix (ECM)
Ud over disse ni kendetegn for aldring, som blev defineret i 2013, er der et tiende kendetegn på vej. To forskere, Alexander Fedintsev og Alexey Moskalev, har udgivet en artikel i 2021, der ser nærmere på stivhed i den ekstracellulære matrix (ECM): opbygningen af tværbindinger mellem langtidsholdbare molekyler som kollagen og elastin. De foreslår, at ECM-afstivning er forårsaget af de ikke-enzymatiske kemiske reaktioner glykering, carbamylering og carbonylering, og at det endda kan være den forudgående årsag til flere accepterede kendetegn ved aldring, såsom cellulær senescens.. Disse ændringer fører til dannelse af addukter og krydsbindinger, som igen forårsager inflammation, fibrose, forstyrrelse af vævets døgnrytme, aldring af stamceller og så videre. Det er tidligere blevet fastslået, at avancerede glykationsendeprodukter (AGE'er) har patogen betydning for forskellige væv og veje i kroppen. Organismer med ekstraordinær lang levetid (som grønlandshvaler) har usædvanligt lav ophobning af AGE'er.
Potentielle behandlingsformer til ekstracellulær matrix (ECM) stivhed (Hallmark #10):
I menneskelige skeletmuskler skyldes den aldersrelaterede funktionsnedsættelse øget stivhed af ECM, hovedsageligt forårsaget af kollagenakkumulering.
- Manuel terapi og mekanistisk tryk
- Osteopatisk terapiAkupunktur, myofascial release
- En kombination af syntetiske og naturlige AGE-hæmmere arbejder synergistisk på forskellige stadier af dannelsen
- Naturlige produkter omfatter carnosin, alfa-liponsyre, taurin, C-vitamin, benfotiamin og pyridoxamin ->. Produktanbefaling
- Polyfenoler, terpenoider og polysaccharider
- Reducer også indtaget af avancerede glykationsslutprodukter fra fødevarer
- Stimulere elastogenese (nye lægemidler?)
- RAGE-antagonister (receptor for avancerede glykationsslutprodukter) [forskellige peptider].
///








