Das Studium der Belastbarkeit durch die Linse der Genetik ist ein wachsendes Interessensfeld, das sich häufig mit den Disziplinen der Psychologie, Neurobiologie und Genomik überschneidet. Während das Konzept der Widerstandsfähigkeit - die Fähigkeit, Widrigkeiten oder Stress zu erholen oder sich anzupassen - facettenreich ist und durch ein komplexes Zusammenspiel von genetischen, ökologischen und psychologischen Faktoren beeinflusst werden, wurden spezifische DNA -Tests entwickelt, um Licht auf die genetischen Komponenten davon zu bringen Eigenschaft.
Einführung
Gene sind DNA -Segmente, die die Anweisungen enthalten, die der Körper benötigt, um jedes der vielen Tausenden von Proteinen für das Leben erforderlich zu machen. Jedes Gen umfasst Tausende von Kombinationen von "Buchstaben" (als Basen genannte Basen), die Ihren genetischen Code bilden. Der Code gibt die Anweisungen, um die für die ordnungsgemäße Entwicklung und Funktion erforderlichen Proteine zu erstellen.(1)
Genetische Variationen können die Expression eines Gens beeinflussen und damit Stoffwechselprozesse beeinflussen, die für die Aufrechterhaltung der zellulären Gesundheit und der Reaktion auf Umweltinterventionen wie Ernährung, Lebensstil, Nahrungsergänzungsmittel und Medikamente wichtig sind.
Die Kenntnis dieser genetischen Variationen bietet beispiellose Einblicke in biologische Systeme und ermöglicht es den Arztpraktikern, präzise Interventionen zu empfehlen, die darauf abzielen, die eigenen Ziele zu erreichen und eine optimale Gesundheit zu erreichen.
Genetische Marker der Belastbarkeit verstehen
Widerstandsfähigkeit- Die Fähigkeit, sich von Widrigkeiten oder Veränderungen leicht zu erholen oder sie anzupassen, wird zunehmend durch die Genetik gesehen. Durch die Untersuchung von genetischen Markern wollen Forscher und Kliniker die biologischen Grundlagen aufdecken, die erklären könnten, warum einige Personen von Stress und Trauma effektiver abprallen als andere.(2) Dieser aufstrebende Untersuchungsgebiet konzentrierte sich auf resilienzbedingte DNA-Tests, die genetische Marker untersuchen, die potenziell für die Unterschiede in den individuellen Stressreaktionen verantwortlich sind.
Im Zentrum dieser Forschung liegt das endokrine und Nervensystem (insbesondere das autonome Nervensystem) zentral zur Reaktion des Körpers auf Stress. Insbesondere die Hypothalamus-Hypophysen-Nebennieren-Achse (HPA) ist ein zentraler Fokusbereich, da sie eine entscheidende Rolle bei der Regulierung des Stressantwortmechanismus des Körpers spielt. Dieses komplexe Netzwerk von Wechselwirkungen zwischen dem Hypothalamus, der Hypophyse und den Nebennierendrüsen orchestriert die Produktion und Regulation von Schlüsselstresshormonen wie Cortisol.
Cortisol hat weitreichende Auswirkungen auf viele körperliche Funktionen und wird als Reaktion auf Stress und niedrige Blutglucosekonzentration freigesetzt. Unter normalen Umständen hilft Cortisol bei der Wiederherstellung der Homöostase nach stressigen Ereignissen. Genvariationen, die die HPA -Achse beeinflussen, können jedoch zu Unterschieden in der Erzeugung, Regulierung und Entfernen von Cortisol aus dem Körper führen. Diese genetischen Variationen können die physiologische Widerstandsfähigkeit eines Individuums beeinflussen - ihre Fähigkeit, nach Schwierigkeiten auf die psychische und körperliche Gesundheit zurückzukehren oder schnell zurückzukehren.(3)
DNA -Tests auf Belastbarkeit Untersuchen Sie Genvarianten, die mit den Rezeptoren für Stresshormone assoziiert sind, Proteine, die an den Stresshormonwegen und Enzymen beteiligt sind, die diese Hormone metabolisieren. Beispielsweise könnte eine Variante des FKBP5-Gens, die an der Regulierung der Empfindlichkeit des Glukokortikoidrezeptors beteiligt ist, durch den Cortisol seine Auswirkungen ausübt, die Stressreaktion eines Individuums und möglicherweise ihre Anfälligkeit für stressbedingte Störungen verändern. Die Erweiterung des Umfangs, Gene, die für Neurotransmitter kodieren - die chemischen Boten des Gehirns, die zur Stimmungsregulation und Erkenntnis beitragen - stehen ebenfalls im Rampenlicht. Dazu gehören Gene wie COMT, das maßgeblich am Abbau von Dopamin beteiligt ist, einem Neurotransmitter, der mit Vergnügungs- und Belohnungssystemen assoziiert ist.(4)
Zusätzlich, Entzündung ist ein biologischer Prozess, der eng mit Stress- und Stimmungsstörungen verbunden ist. Chronische Entzündungen, die genetische Variationen beeinflussen können, kann die Gehirnfunktion und das Gehirn beeinflussen.(5) Daher können Gentests auch versuchen, Varianten in proinflammatorischen Zytokin-Genen wie IL-6 und TNF zu identifizieren, die Individuen für die Verlängerung entzündlicher Reaktionen und die Beeinflussung ihrer geistigen Belastbarkeit könnten.
Das Verständnis dieser genetischen Marker ist der Eckpfeiler für personalisierte Interventionen. Durch die Identifizierung genetischer Veranlagungen können Einzelpersonen proaktive Schritte unternehmen, um ihre Widerstandsfähigkeit durch Veränderungen des Lebensstils, psychologische Strategien und medizinische Behandlungen zu stärken, die auf ihr einzigartiges genetisches Make -up zugeschnitten sind. Dieser Ansatz veranschaulicht die Verschiebung in Richtung Präzisionsmedizin, bei dem das einheitliche Modell der individuelleren Versorgung weichen.
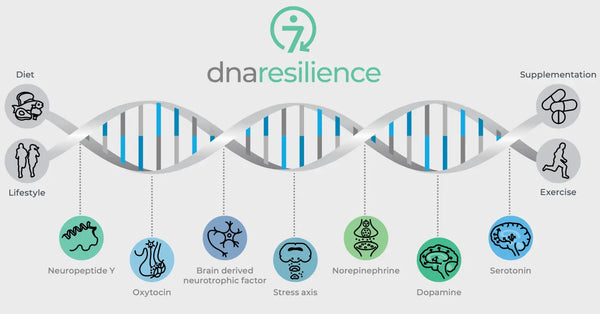
Bild: Die sieben molekularen Wege der Belastbarkeit.
Arten von DNA -Tests auf Belastbarkeit
1) Spannungsantwortgene
Gene der Stressreaktion sind kritische Bestandteile des Körpersystems für die Verwaltung und Reaktion auf Stressoren. Sie kodieren Proteine, die verschiedene physiologische Prozesse regulieren, einschließlich der Freisetzung und Wirkung von Cortisol, einem Hormon -zentralen bei der Stressreaktion.
CRHR1 (Corticotropin-freisetzender Hormonrezeptor 1)
CRHR1 codiert einen Rezeptor für Corticotropin-Releasing-Hormon (CRH), ein zentrales Hormon, das die Stressreaktion initiiert. Wenn CRH an CRHR1 bindet, stimuliert es die Produktion und Freisetzung von Adrenocorticotropenhormon (ACTH), was die Nebennierendrüsen zur Herstellung von Cortisol veranlasst. Varianten im CRHR1 -Gen können beeinflussen, wie empfindlich dieser Rezeptor für CRH ist, was die Gesamtspannungsreaktion verändern kann. Zum Beispiel könnten einige Polymorphismen zu einer erhöhten Stressreaktion führen, die zu Angstzuständen oder Depressionen beitragen könnte. Im Gegensatz dazu können andere die Reaktion dämpfen und sich auf die Fähigkeit auswirken, mit akutem Stress umzugehen.(6-7)
FKBP5 (FK506 -Bindungsprotein 5)
Das FKBP5 -Gen spielt eine Rolle bei der Regulierung der Empfindlichkeit des Glukokortikoidrezeptors, dem Rezeptor, durch den Cortisol seine Wirkungen ausübt. Spezifische Polymorphismen in FKBP5 wurden mit einer veränderten Rückkopplungshemmung der HPA -Achse und der unterschiedlichen Reaktionen auf Glukokortikoide in Verbindung gebracht. Beispielsweise können einige Varianten von FKBP5 die Affinität des Glukokortikoidrezeptors für Cortisol verringern, was möglicherweise zu einer beeinträchtigten Stressreaktion und einem erhöhten Risiko für stressbedingte psychiatrische Erkrankungen wie PTBS oder Major Depression führt.(8-9)
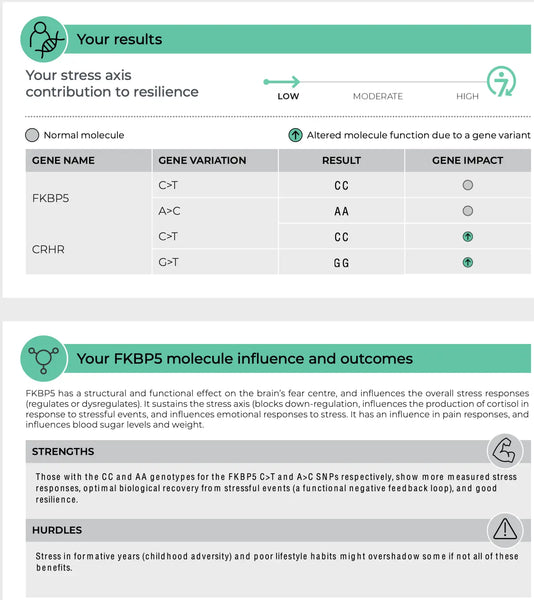
Bild: Eine Beispielseite der DNA -Resilienz -Test.
NR3C1 (Unterfamilie der Kernrezeptor 3, Gruppe C, Mitglied 1)
NR3C1 codiert den Glukokortikoidrezeptor selbst. Variationen in diesem Gen können beeinflussen, wie der Körper auf Cortisol reagiert. Spezifische Polymorphismen in NR3C1 können die Empfindlichkeit oder Dichte von Glukokortikoidrezeptoren beeinflussen, was beeinflusst, wie effektiv Cortisol seine Funktionen ausführen kann. Dies kann zu einer Reihe von Reaktionen führen, von einer gedämpften Stressreaktion, die eine Person daran hindert, angemessen auf Stressoren zu einer übertriebenen Reaktion zu reagieren, die zu chronischen Stresssymptomen und sogar zu Depressionen führen kann.(10-12)
Die Ergebnisse aus den Tests der Stressreaktionsgen können Einblicke in die Veranlagung eines Individuums zu stressbedingten Gesundheitsproblemen geben. Zum Beispiel:
-
Erhöhte Stressreaktion: Personen mit spezifischen Varianten könnten bei stressigen Ereignissen auf Stress reagierter sein und höhere Cortisolspiegel erleben.
-
Reduzierte Stressreaktion: Umgekehrt könnten einige Personen eine abgestumpfte Stressreaktion haben, die in akuten Stresssituationen schützend sein könnte, aber auch die Aktivierung der notwendigen physiologischen Mechanismen als Reaktion auf Herausforderungen behindern könnte.
2) Neurotransmitter -Funktionstests erklärt
Neurotransmitter -Funktionstests sollen die genetischen Faktoren untersuchen, die beeinflussen, wie Neurotransmitter im Gehirn synthetisiert, freigesetzt und abgebaut werden. Da Neurotransmitter chemische Boten sind, die die Stimmung, die Wahrnehmung und die Stressreaktionen regulieren, können Variationen der mit diesen Substanzen verbundenen Gene erhebliche Auswirkungen auf die psychologische Belastbarkeit und die allgemeine psychische Gesundheit eines Individuums haben.
Die Erforschung der Neurotransmitterfunktion im Kontext von Belastbarkeit und Stressreaktion erstreckt sich über die Katecholamine wie Dopamin hinaus. Es umfasst ein breiteres Spektrum von Neurotransmittersystemen, die an der Stimmungsregulation, der Wachsamkeit und der kognitiven Funktion beteiligt sind. Mehrere Gene sind an der Synthese, Signalübertragung und Abbau dieser Neurotransmitter beteiligt, einschließlich Dopamin-Beta-Hydroxylase (DBH), Dopaminrezeptoren (DRD2, DRD4) und verschiedenen serotoninbezogenen Genen.(13)
COMT (Catechol-o-Methyltransferase)
Das COMT -Gen ist eines der am weitesten untersuchten Neurotransmitterfunktionen. Es codiert ein Enzym, das Katecholamine - wie Dopamin, Adrenalin und Noradrenalin - abschließt.
Es gibt bekannte Polymorphismen im COMT-Gen wie die Val158met-Variante. Diese Variante kann das Aktivitätsniveau des Enzyms auf unterschiedliche Weise beeinflussen:(14-15)
- Hochaktivitätsform (VAL-Variante): Diese Form des Enzyms bricht Dopamin schneller auf, was zu niedrigeren Dopaminspiegeln im präfrontalen Kortex führen kann, einer Gehirnregion, die an der Exekutivfunktion und der Entscheidungsfindung beteiligt ist. Personen mit dieser Variante können bei Aufgaben unter stabilen Bedingungen besser abschneiden, sind jedoch aufgrund der geringeren Verfügbarkeit von Dopamin anfälliger für den kognitiven Rückgang unter Stress.
- Niedrigaktivitätsform (MET-Variante): Umgekehrt metabiert diese Form des COMT -Enzyms Dopamin langsamer, was zu höheren Dopaminspiegeln im Gehirn führt. Dies kann die kognitive Funktion unter Stress verbessern, kann jedoch auch das Risiko von stressbedingten Psychopathologien wie Angststörungen erhöhen, da das Gehirn möglicherweise durch überschüssiges Dopamin überstimuliert wird.
Dopamin Beta-Hydroxylase (DBH)
DBH ist ein Enzym, das Dopamin in Norepinephrin umwandelt, einem Neurotransmitter, der an der Reaktion des Kampfes oder Flugs beteiligt ist. Genetische Variationen im DBH -Gen können die Enzymaktivität beeinflussen und die Dopamin- und Noradrenalinspiegel im Gehirn und im peripheren Nervensystem beeinflussen.(16-18)
- Niedrige Aktivität: Varianten, die mit einer niedrigeren DBH-Aktivität verbunden sind, können zu höheren Dopaminspiegeln und verringerten Noradrenalnenniveaus führen, die sich auf kognitive Funktionen wie Aufmerksamkeit und Entscheidungsfindung auswirken und beeinflussen, wie ein Individuum auf Stress reagiert.
- Hohe Aktivität: Umgekehrt können Varianten, die zu einer höheren DBH -Aktivität führen, die Dopaminspiegel senken und gleichzeitig die Noradrenalin erhöhen und möglicherweise die Stressreaktivität und Angstzustände beeinflussen.
Dopaminrezeptoren (DRD2 und DRD4)
DRD2 und DRD4 sind Gene, die Dopaminrezeptoren D2 bzw. D4 codieren. Diese Rezeptoren sind Teil des Dopamin -Systems, das zahlreiche Funktionen reguliert, einschließlich Stimmung, Belohnung und motorischer Kontrolle.19-20)
- DRD2: Varianten im DRD2 -Gen können die Dichte und die Bindungsaffinität von D2 -Rezeptoren beeinflussen. Dies kann die Anfälligkeit für Stress und die Wirksamkeit von Belohnungshinweisen beeinflussen, was potenzielle Auswirkungen auf Erkrankungen wie Sucht und Depressionen hat.
- DRD4: Das DRD4 -Gen ist für eine variable Anzahl von Tandem -Wiederholungen (VNTR) in der Codierungsregion bekannt. Spezifische Wiederholungen sind mit Merkmalen wie Neuheitssuche und dem Risiko für Aufmerksamkeitsstörungen verbunden. Dieser Polymorphismus kann die Effizienz der synaptischen Dopamin -Signalübertragung beeinflussen und im Kontext von Verhaltens- und psychologischer Belastbarkeit untersucht.
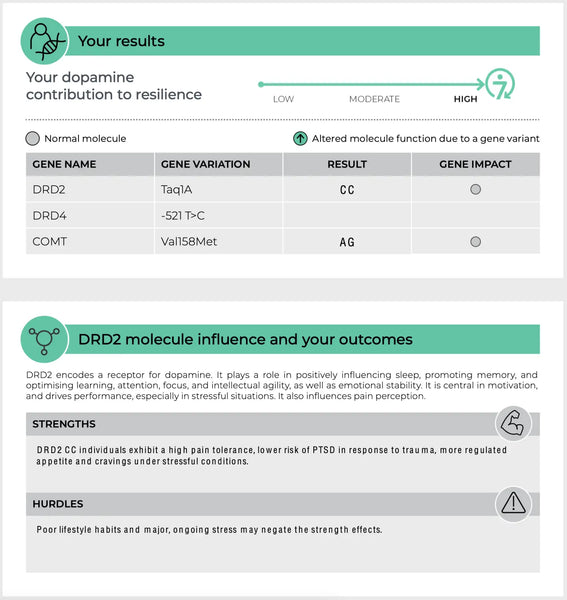
Bild: Eine Beispielseite der DNA -Resilienz -Test.
Serotonin -Genvariationen
Serotonin ist ein weiterer entscheidender Neurotransmitter bei der Regulierung von Stimmung, Appetit und Schlaf, die alle durch Stress beeinflusst werden können. Mehrere Gene, die an der Serotonin -Signalübertragung beteiligt sind, sind von Interesse:
- 5-HTT (SLC6A4): Dieses Gen codiert den Serotonintransporter, der für die Wiederaufnahme der Serotonin aus der synaptischen Spalte verantwortlich ist. Der 5-HTTLPR-Polymorphismus in der Promotorregion dieses Gens wurde für seinen Zusammenhang mit Stressempfindlichkeit und Stimmungsstörungen untersucht.(21)
- Maoa: Die Monoaminoxidase Ein Gen ist dafür verantwortlich, Serotonin abzubauen. Variationen in diesem Gen können die Serotoninspiegel beeinflussen und mit Verhaltensmerkmalen und Stressanfälligkeit in Verbindung gebracht wurden.(22)
- TPH2: Tryptophan Hydroxylase-2 ist ein Enzym, das für die Synthese von Serotonin im Gehirn kritisch ist. Genetische Variationen in TPH2 können die Serotoninproduktion beeinflussen und möglicherweise die emotionale Regulierung und die Reaktion auf Stress beeinflussen.(23)
Die Interpretation von Ergebnissen aus diesen Tests kann komplex sein. Beispielsweise bedeutet eine Variante, die mit einem höheren Risiko für stressbedingte Bedingungen verbunden ist, nicht unbedingt, dass ein Individuum solche Bedingungen entwickelt, aber möglicherweise auf eine erhöhte Anfälligkeit hinweist. In ähnlicher Weise garantiert der Besitz einer "Resilienz" -Variante keinen unangemessenen Widerstand gegen Stress, da Umweltfaktoren und Lebensstilentscheidungen erhebliche Rollen spielen.
3) Entzündung und ihre Auswirkungen auf das Gehirn
Eine chronische Entzündung kann sich nachteilig auf die Gesundheit des Gehirns auswirken. Es wird angenommen, dass es zur Entwicklung und dem Fortschreiten neurodegenerativer Erkrankungen beiträgt und die Stressreaktion des Gehirns beeinflussen kann, die eng mit der Widerstandsfähigkeit verbunden ist. Proinflammatorische Zytokine wie Interleukin-6 (IL-6) und Tumornekrosefaktor (TNF) können die Blut-Hirn-Barriere überqueren und mit den Wegen interagieren, die Stimmung, Motivation und Wachsamkeit regulieren.(24)
Genvarianten, die mit Entzündungen verbunden sind
IL-6 (Interleukin-6)
IL-6 ist ein Zytokin, das eine Rolle bei der Entzündungsreaktion spielt und an verschiedenen biologischen Funktionen beteiligt ist, einschließlich der Immunantwort, der Hämatopoese und des Knochenstoffwechsels. Im Kontext von Stress und Belastbarkeit hängt IL-6 mit Folgendem zusammen:(25-26)
- Erhöhte IL-6-Spiegel wurden mit einem höheren Risiko für die Entwicklung von Depressionen und anderen Stimmungsstörungen in Verbindung gebracht.
- Spezifische genetische Varianten des IL-6-Gens können zu einer erhöhten Expression von IL-6 führen, die möglicherweise die Entzündungsreaktion verschlimmern und die Fähigkeit des Gehirns, mit Stress umzugehen, verändert.
TNF (Tumornekrosefaktor)
TNF ist ein weiteres Zytokin, das an systemischer Entzündung beteiligt ist. Es hat verschiedene Rollen, einschließlich der Regulierung von Immunzellen und der Induktion von Fieber, Apoptose und Entzündung.(27)
- Die Überexpression von TNF wurde mit verschiedenen chronischen Krankheiten in Verbindung gebracht, einschließlich rheumatoider Arthritis, entzündlicher Darmerkrankungen und Psoriasis sowie psychischer Stress und Depressionen.
- Varianten im TNF -Gen können das Niveau der TNF -Produktion beeinflussen, was direkte Auswirkungen auf entzündliche Prozesse im gesamten Körper und im Gehirn haben kann.
4) Neurobiologische Regulatoren und Resilienzfaktoren
Genetische Variationen in entscheidenden neurobiologischen Regulatoren regeln auch die Widerstandsfähigkeit gegenüber Stress. Dazu gehören Oxytocin, der von Hirn abgeleitete neurotrophe Faktor (BDNF) und Neuropeptid Y (NPY). Oxytocin spielt eine Rolle bei der Regulierung sozialer Verhaltensweisen und Stressreaktionen. BDNF ist entscheidend für die Aufrechterhaltung der Neuroplastizität und der kognitiven Funktion unter Stress, und NPY moduliert die Angst und die physiologische Stressreaktion. Diese Moleküle beeinflussen gemeinsam unsere neuronalen Schaltkreise und unsere psychologische Widerstandsfähigkeit und geben Einblicke in individuelle Unterschiede in der Belastbarkeit von Stress und potenziellen Möglichkeiten für personalisierte Biohacking -Strategien.
Oxytocin
Oxytocin wird oft als "Liebeshormon" bezeichnet, weil es bei sozialer Bindung, mütterlicher Verhalten und Intimität in der sozialen Bindung, mütterlicher Verhaltensweisen und Intimität ist. Es übt auch anxiolytische Wirkungen aus und beeinflusst soziale Kognition und Verhalten.
- Genetischer Einfluss: Variationen des Oxytocin -Rezeptor -Gens (OXTR) wurden mit emotionaler Regulierung, soziales Verhalten und Stressreaktionsfähigkeit in Verbindung gebracht. Spezifische Polymorphismen in OXTR können die Bindungseffizienz und die Expressionsniveaus von Oxytocin -Rezeptoren beeinflussen, die die Fähigkeit eines Individuums beeinflussen können, mit Stress umzugehen und soziale Beziehungen zu formen.(28)
- Implikationen: Im Zusammenhang mit Resilienztests kann die Beurteilung von OXTR -Varianten Einblicke in die Veranlagung eines Individuums für soziale Angst, Empathie und potenzielle Belastbarkeit angesichts von Stress liefern, insbesondere für die soziale Dynamik.(29)
Der von Gehirn abgeleitete neurotrophe Faktor (BDNF)
BDNF ist ein entscheidendes Protein, das an der Neuroplastizität beteiligt ist, die Fähigkeit des Gehirns, während des gesamten Lebens neue neuronale Verbindungen neu zu organisieren und zu formen. Es ist entscheidend für das Lernen, Gedächtnis und die Regeneration von Neuronen.(30)
- Genetische Variationen: Die BDNF -Genvariante Val66met ist einer der am meisten untersuchten Polymorphismen. Das Met-Allel wurde mit einer verringerten Aktivitätsabhängigkeit von BDNF in Verbindung gebracht, die die kognitive Funktion und Widerstandsfähigkeit gegenüber neurologischen und psychiatrischen Erkrankungen beeinflussen könnte.(31)
- Implikationen: Die Tests auf BDNF -Genvarianten könnten dazu beitragen, die Fähigkeit eines Individuums zur Neuroplastizität als Reaktion auf Stress vorherzusagen und Auswirkungen auf die Erholung von neurologischen Beleidigungen oder Trauma haben.(32)
Bild: Eine Beispielseite der DNA -Resilienz -Testanalyse.
Neuropeptid Y (NPY)
NPY ist eines der am häufigsten vorkommenden Peptide im Gehirn und ist an der Regulierung von Stressreaktionen, Angstzuständen und Nahrungsaufnahme beteiligt. Es wird als endogenes anxiolytisches Mittel angesehen.
- Genetische Assoziationen: Polymorphismen im NPY -Gen können zu Unterschieden in der NPY -Expression und -sekretion führen, die möglicherweise die Stressresilienz eines Individuums beeinflussen. Höhere NPY -Werte schützen im Allgemeinen vor den Auswirkungen von Stress.
- Implikationen Gentests für NPY -Varianten können möglicherweise auf die Widerstandsfähigkeit der Basisstress des Individuums hinweisen und ihre psychologische Reaktion auf chronischen Stress und Trauma vorhersagen.(33)
Die Rolle der Epigenetik bei der Modulation der Belastbarkeit von Stress
Das Feld von Epigenetik befasst sich in eine Komplexitätsschicht jenseits der statischen DNA -Sequenz. Epigenetische Modifikationen bestehen aus chemischen Veränderungen der DNA -Struktur wie Methylierungs- und Histonmodifikationen, die sich auswirken können, wie Gene exprimiert werden, ohne den zugrunde liegenden genetischen Code zu verändern. Diese Veränderungen sind dynamisch und reagieren auf Umweltreize, einschließlich chronischer Stress. Die Exposition gegenüber längerer Stress kann zu epigenetischen Veränderungen führen, die die Funktionsweise von Genen beeinflussen, die an der Stressreaktion beteiligt sind, und es möglicherweise schwieriger macht, neue Stressoren effektiv umzugehen.(34-35)
Unternehmen an der Spitze der personalisierten Medizin wagen sich nun in die Epigenetik und versuchen, herauszufinden, wie diese Modifikationen zur Fähigkeit eines Einzelnen beitragen können, aus Stress zu standhalten und zurückzuschwingen. Durch die Analyse epigenetischer Marker können Wissenschaftler Einblicke in den aktuellen Zustand der Genexpressionsprofile gewinnen, die sowohl aus genetischen Veranlagungen als auch aus Umwelteinflüssen resultieren. Solche Tests können epigenetische Veränderungen als Reaktion auf chronischen Stress identifizieren und eine Momentaufnahme der molekularen Mechanismen liefern, die zur Stressreaktion oder dessen Fehlen eines Individuums beitragen.
Darüber hinaus öffnet das Verständnis dieser epigenetischen Veränderungen die Tür zu personalisierten Interventionen. Spezifische Veränderungen des Lebensstils, Ernährungsanpassungen und therapeutische Strategien können empfohlen werden, um unerwünschte epigenetische Modifikationen umzukehren. Dieser personalisierte Ansatz verbessert nicht nur die Widerstandsfähigkeit eines Individuums, sondern trägt auch zu einem umfassenderen Verständnis, wie Stress auf epigenetische Ebene auf unsere biologischen Systeme auswirkt, was zu neuen Behandlungen und vorbeugenden Strategien für stressbedingte Störungen führen könnte. Durch die Kartierung der epigenetischen Landschaft der Stressreaktion können wir beginnen, ein umfassenderes Bild der Faktoren zu malen, die zu unserer einzigartigen Fähigkeit beitragen, mit den Herausforderungen des Lebens umzugehen.
Die Vorteile und Einschränkungen von Resilienz -DNA -Tests
Diese Tests können Einzelpersonen ein besseres Verständnis für ihre angeborene Belastbarkeit und Stressreaktion bieten. Ein solches Wissen könnte personalisierte Strategien zur Behandlung von Stress und zur Verbesserung der psychischen Gesundheit beeinflussen. Es ist jedoch wichtig, diese Tests mit Vorsicht zu nähern:
- Komplexes Merkmal: Resilienz wird nicht durch ein einzelnes Gen bestimmt, ist jedoch ein komplexes Merkmal, das von vielen Genen und Umweltfaktoren beeinflusst wird.
- Umwelteinfluss: Die Genetik funktioniert nicht isoliert. Lebenserfahrungen, Unterstützungssysteme und Lebensstilentscheidungen sind in Belastbarkeit von Bedeutung.
- Vorhersagekraft: Während diese Tests Einblicke liefern können, sind sie keine endgültigen Prädiktoren für die Fähigkeit eines Individuums, die Herausforderungen des Lebens zu bewältigen.
Abschluss
DNA -Tests im Zusammenhang mit Resilienz sind eine faszinierende Grenze, um zu verstehen, wie unser genetisches Make -up die Fähigkeit beeinflussen könnte, mit Stress umzugehen und sich von Widrigkeiten zu erholen. Während sie wertvolle Erkenntnisse liefern können, sollten sie als ein Stück des riesigen Puzzles angesehen werden, das die Widerstandsfähigkeit eines Individuums darstellt. Für alle, die an diesen Tests interessiert sind, wird empfohlen, einen Gesundheitsdienstleister oder einen genetischen Berater zu beraten, um die Ergebnisse im breiteren Kontext ihrer Gesundheit und ihres Lebensstils zu interpretieren.
- Holen Sie sich Ihren integralen DNA -Test hier!
- Buchen Sie hier eine Beratung, um Ihr Labor- und Gentests mit Dr. Sovijärvi zu interpretieren.
Wissenschaftliche Referenzen:
- Bobrow, M. & Grimbaldeston, A. H. (2000). Medical Genetics, The Human Genome Project and Public Health: Präsentiert an der University of Liverpool, 9. Dezember 1996 und am 17. Februar 2000 zur Veröffentlichung angenommen. Journal of Epidemiology & Community Health, 54 (9), 645-649.
- Cicchetti, D. (2010). Resilienz unter Bedingungen extremer Stress: eine mehrstufige Perspektive. World Psychiatry, 9 (3), 145.
- Luecken, L. J. & Gallo, L. C. (Hrsg.). (2008). Handbuch für physiologische Forschungsmethoden in der Gesundheitspsychologie. Salbei.
- Southwick, S. M., Vythilingam, M. & Charney, D. S. (2005). Die Psychobiologie von Depressionen und Belastbarkeit gegen Stress: Auswirkungen auf die Prävention und Behandlung. Annu. Rev. Clin. Psychol., 1, 255-291.
- M. Proinflammatorische Zytokine, Altern und altersbedingte Krankheiten. Journal of the American Medical Directors Association, 14 (12), 877-882.
- G. Aguilera, M. Nikodemova, P. C. Wynn & K. J. Catt (2004). Corticotropin Freisetzung Hormonrezeptoren: Zwei Jahrzehnte später. Peptide, 25 (3), 319-329.
- T. Subbannayya, L. Balakrishnan, G. Sudarshan, J. Advani, S. Kumar, R. Mahmood, T. K. (2013). Eine integrierte Karte des Corticotropin-Releasing-Hormon-Signalwegs. Journal of Cell Communication and Signaling, 7, 295-300.
- Binder, E. B. (2009). Die Rolle von FKBP5, einem Co-Chaperon des Glukokortikoidrezeptors bei der Pathogenese und Therapie von affektiven und Angststörungen. Psychoneuroendocrinology, 34, S186-S195.
- Ising, M., Depping, A. M., Siebe, A., Lucae, S., Unschmud, P. G., Kloiber, S., ... & Holsboer, F. (2008). Polymorphismen in der FKBP5 -Genregion modulieren die Erholung von psychosozialem Stress bei gesunden Kontrollen. European Journal of Neuroscience, 28 (2), 389-398.
- G. Vitellius, S. Trabado, J. Bouligand, B. Delemer & M. Lombès (2018, Juni). Pathophysiologie der Glukokortikoid -Signalübertragung. In Annales d'Entocrinologie (Band 79, Nr. 3, S. 98-106). Elsevier Masson.
- Van West, D., Van Den Eede, F., Del-Favero, J., Souery, D., Norrback, K. F., Van Duijn, C., ... & Claes, S. (2006). SNP-basierte SNP-Analyse von Glucocorticoidrezeptor bei Patienten mit wiederkehrender Hauptdepression. Neuropsychopharmacology, 31 (3), 620-627.
- K. K. Schneider, C. Frings, J. Meyer & A. B. Schote (2016). Die Rolle des Glukokortikoidrezeptor -Gens (NR3C1) für die Verarbeitung von aversiven Stimuli. Neurowissenschaftsforschung, 107, 8-13.
- Azadmarzabadi, E., Haghighatfard, A. & Mohammadi, A. (2018). Eine geringe Belastbarkeit gegen Stress ist mit Veränderungen der Kandidatengenexpression im dopaminergen Signalweg verbunden. Psychogeriatrie, 18 (3), 190-201.
- HEinz, A. & Smolka, M. N. (2006). Die Auswirkungen des Catechol-O-Methyltransferase-Genotyps auf die Aktivierung des Gehirns, die durch affektive Stimuli und kognitive Aufgaben hervorgerufen wurden. Bewertungen in den Neurowissenschaften, 17 (3), 359-368.
- Mier, D., Kirsch, P. & Meyer-Lindenberg, A. (2010). Neuronale Substrate pleiotroper Wirkung genetischer Variation in COMT: Eine Metaanalyse. Molekulare Psychiatrie, 15 (9), 918-927.
- Mustapic, M., Maihofer, A. X., Mahata, M., Chen, Y., Baker, D. G., O'Connor, D. T. & Nievergelt, C. M. (2014). Das Catecholamin-Biosynthese-Enzym Dopamin-β-Hydroxylase (DBH): Erste genomweite Suchpositionspositionen Merkmalsbestimmende Varianten, die additiv im proximalen Promotor wirken. Human Molecular Genetics, 23 (23), 6375-6384.
- Vincent, S. & Robertson, D. (2002). Die breitere Sichtweise: Katecholamin -Anomalien. Klinische autonome Forschung, 12, I44-I49.
- J. Hoenicka, M. Aragüés, G. Ponce, R. Rodríguez-Jiménez, M. A. Jiménez-Arriero & T. Palomo (2007). Von dopaminergen Genen bis hin zu psychiatrischen Störungen. Neurotoxizitätsforschung, 11, 61-71.
- Hill, S. Y., Hoffman, E.K., Zezza, N., Thalamuthu, A., Weeks, D. E., Matthews, A. G. & Mukhopadhyay, I. (2008). Dopaminerge Mutationen: Assoziation innerhalb der Familie und Verknüpfung in Familien mit Multiplex -Alkoholabhängigkeit. American Journal of Medical Genetics Teil B: Neuropsychiatrische Genetik, 147 (4), 517-526.
- Er, Y., Martin, N., Zhu, G. & Liu, Y. (2018). Kandidatengene für Neuheitssuche: Eine Metaanalyse von Assoziationsstudien von: DRD4: Exon III und: Comt: Val158met. Psychiatrische Genetik, 28 (6), 97-109.
- Avula, R., Rand, A., Black, J. L. & O'Kane, D. J. (2011). Simultane Genotypisierung mehrerer Polymorphismen im menschlichen Serotonintransportergen und Nachweis neuer Allelvarianten. Translationale Psychiatrie, 1 (8), E32-E32.
- E. A. Tivol, C. Shalish, D. E. Schuback, Y. P. Hsu & X. O., Breakefield (1996). Mutationsanalyse des menschlichen Maoa -Gens. American Journal of Medical Genetics, 67 (1), 92-97.
- J. Wader, N. Araragi, L. Gutknecht & K. P. Lesch (2011). Tryptophan Hydroxylase-2 (TPH2) bei Erkrankungen der kognitiven Kontrolle und der Regulierung von Emotionen: eine Perspektive. Psychoneuroendocrinology, 36 (3), 393-405.
- Bauer, M. E. & Teixeira, A. L. (2021). Neuroinflammation bei Stimmungsstörungen: Rolle regulatorischer Immunzellen. Neuroimmunomodulation, 28 (3), 99-107.
- Anderson, G., Kubera, M., Duda, W., Lasoń, W., Berk, M. & Maes, M. (2013). Erhöhte IL-6-Transsignalisierung der Depression: Konzentrieren Sie sich auf den Tryptophan-Katabolitenweg, Melatonin und Neuroprogression. Pharmakologische Berichte, 65 (6), 1647-1654.
- Perry, B. I., Upthegrove, R., Kappelmann, N., Jones, P. B., Burgess, S. & Khandaker, G. M. (2021). Assoziationen von immunologischen Proteinen/Merkmalen mit Schizophrenie, Major Depression und bipolare Störung: Eine bidirektionale Mendelian-Randomisierungsstudie mit zwei Stichproben. Gehirn, Verhalten und Immunität, 97, 176-185.
- Bradley, J. (2008). TNF -vermittelte entzündliche Erkrankung. Das Journal of Pathology: Ein Journal der Pathologischen Gesellschaft Großbritanniens und Irlands, 214 (2), 149-160.
- LOth, E., Poline, J. B., Thyreau, B., Jia, T., Tao, C., Lourdusamy, A., ... & Imagin Consortium. (2014). Der Genotyp des Oxytocinrezeptors moduliert die ventrale striatale Aktivität auf soziale Hinweise und die Reaktion auf stressige Lebensereignisse. Biologische Psychiatrie, 76 (5), 367-376.
- Myers, A. J., Williams, L., Gatt, J. M., McAuley-Clark, E. Z., Dobson-Stone, C., Schofield, P. R. & Nemeroff, C. B. (2014). Die Variation des Oxytocin -Rezeptor -Gens ist mit einem erhöhten Risiko für Angstzustände, Stress und Depression bei Personen mit einer Exposition gegenüber dem Stress in frühes Leben verbunden. Journal of Psychiatric Research, 59, 93-100.
- K. K. Cowansage, J. E. Ledoux & M. H. Monfils (2010). Der von Gehirn stammende neurotrophe Faktor: Ein dynamischer Torhüter der neuronalen Plastizität. Aktuelle molekulare Pharmakologie, 3 (1), 12-29.
- Chen, Z. Y., Jing, D., Bath, K. G., Ieraci, A., Khan, T., Siao, C. J., ... & Lee, F. S. (2006). Die genetische Variante BDNF (VAL66MET) -Polymorphismus verändert das an das an das angstbedingte Verhalten. Science, 314 (5796), 140-143.
- Phillips, C. (2017). Der von Gehirn stammende neurotrophe Faktor, Depression und körperliche Aktivität: Die neuroplastische Verbindung herstellen. Neuronale Plastizität, 2017.
- S. N. Schmeltzer, J. P. Herman & R. Sah (2016). Neuropeptid Y (NPY) und posttraumatische Belastungsstörung (PTBS): Ein translationales Update. Experimentelle Neurologie, 284, 196-210.
- Lux, V. (2016, März). Epigenetische Programmierung in der psychobiologischen Entwicklung: Beweise für die Doppelaktivierungstheorie und eine vermittelnde Rolle des Stress in frühes Leben. In der Qatar Foundation Annual Research Conference Proceedings Volume 2016 Ausgabe 1 (Band 2016, Nr. 1, S. Hbop3415). Hamad bin Khalifa University Press (Hbku Press).
- Chukwuma SR, C. (2022). Epigenetik und sein Wesen beim Verständnis des menschlichen Wachstums, der Entwicklung und der Krankheit. J Med Res, 8 (5), 165-172.